Magnijs
Magnijs ir ceturtā visvairāk sastopamā minerālviela cilvēka organismā. Tam ir svarīga loma normālā šūnu funkcionēšanā un dalīšanās procesā, enerģētiskajā vielmaiņā, normālā nervu un muskuļu funkcionēšanā, sirds ritma uzturēšanā un imunitātes veicināšanā. Tiek uzskatīts, ka magnijs atbilstošās devās labvēlīgi iedarbojas uz migrēnu, hroniskām sāpēm, trauksmi un depresiju.
Magnijs ir dabiska minerālviela, kas atklāta 1755. gadā. Tas ir astotais visizplatītākais elements uz zemeslodes, bet dabā tas ir sastopams tikai savienojumu, nevis tīrā veidā. Dabā tas atrodams lielos minerālu nogulumiežos, piemēram, magnezīta un dolomīta iežos.
Magnijs ir nepieciešams visam organismam: muskuļiem, lai tie sarautos, nervu sistēmai, lai tā nosūtītu un saņemtu impulsus. Magnijs nodrošina vienmērīgu sirdsdarbību un stiprina imūnsistēmu.
Magnijs ir būtiska uztura sastāvdaļa, kas ir iesaistīta daudzās svarīgās vielmaiņas reakcijās, piemēram: enerģijas ražošana, glikolīze un nukleīnskābju un olbaltumvielu sintēze.
Tāpat magnijam ir nozīmīga loma arī kalcija un kālija jonu aktīvā transportēšanā caur šūnu membrānām, šim procesam ir būtiska nozīme nervu impulsu vadīšanā, muskuļu saraušanās un normāla sirds ritma nodrošināšanā.
No neiroloģiskā viedokļa, magnijam ir būtiska loma nervu transmisijā un neiromuskulārajā vadībā. Tas arī aizsargā no pārmērīga uzbudinājuma, kas var izraisīt neironu šūnu nāvi (eksitotoksicitāti), un tas savukārt ir saistīts ar dažādiem neiroloģiskiem traucējumiem. Ņemot vērā, cik nozīmīgas ir šīs nervu sistēmas funkcijas, magnijs ir minerālviela, kas izraisījusi īpašu interesi kā neiroloģisko traucējumu iespējamās profilakses un ārstēšanas līdzeklis. Šobrīd pieejamajā zinātniskajā literatūrā tiek apskatīta magnija pielietojamība attiecībā uz migrēnu, hroniskām sāpēm, epilepsiju, Alcheimera, Parkinsona un insulta gadījumiem, kā arī bieži sastopamajiem trauksmes un depresijas stāvokļiem.
Magnijs ir ļoti nozīmīgs mūsu organismam, bet ne visiem cilvēkiem tas ir pietiekamā daudzumā. Kādēļ? Iemesli var būt ļoti dažādi. ASV Nacionālais veselības institūts norāda uz šādām magnija nepietiekamības riska grupām:
Cilvēki ar kuņģa un zarnu trakta slimībām
Hroniska caureja un tauku malabsorbcija, ko izraisa Krona slimība, glutēnsensitīva enteropātija (celiakija) un reģionālais enterīts laika gaitā var izraisīt magnija samazināšanos organismā. Tievās zarnas, īpaši līkumainās zarnas, rezekcija parasti rada uzsūkšanās traucējumus un magnija zudumu.
Cilvēki ar 2. tipa cukura diabētu
Cilvēkiem ar insulīna rezistenci un/vai 2. tipa cukura diabētu var rasties magnija deficīts un pastiprināta magnija izdalīšanās ar urīnu. Magnija zudums, šķiet, ir sekundārs, ja nierēs ir lielāka glikozes koncentrācija, kas palielina urīna daudzumu.
Cilvēki ar alkohola atkarību
Magnija deficīts ir raksturīgs cilvēkiem ar hronisku alkoholismu. Šiem cilvēkiem ir raksturīgi neveselīgi ēšanas ieradumi un neapmierinošs kopējais uzturvielu stāvoklis; kuņģa-zarnu trakta problēmas, tostarp vemšana, caureja un steatoreja (taukaini izkārnījumi), kas rodas pankreatīta dēļ; nieru disfunkcija ar pārmērīgu magnija izdalīšanos urīnā; fosfātu samazināšanās; D vitamīna deficīts; akūta alkohola ketoacidoze; hiperaldosteronisms, kas ir sekundārs pēc aknu slimībām – viss minētais var veicināt magnija samazināšanos organismā.
Gados vecāki cilvēki
Gados vecāki cilvēki magniju ar uzturu uzņem mazāk nekā jaunāki cilvēki. Turklāt ar vecumu samazinās magnija absorbcija zarnās un palielinās tā izdalīšanās caur nierēm. Gados vecākiem cilvēkiem ir arī lielāka iespējamība saslimt ar hroniskām slimībām vai lietot medikamentus, kas izmaina magnija daudzumu organismā, savukārt tas var palielināt magnija deficīta risku.
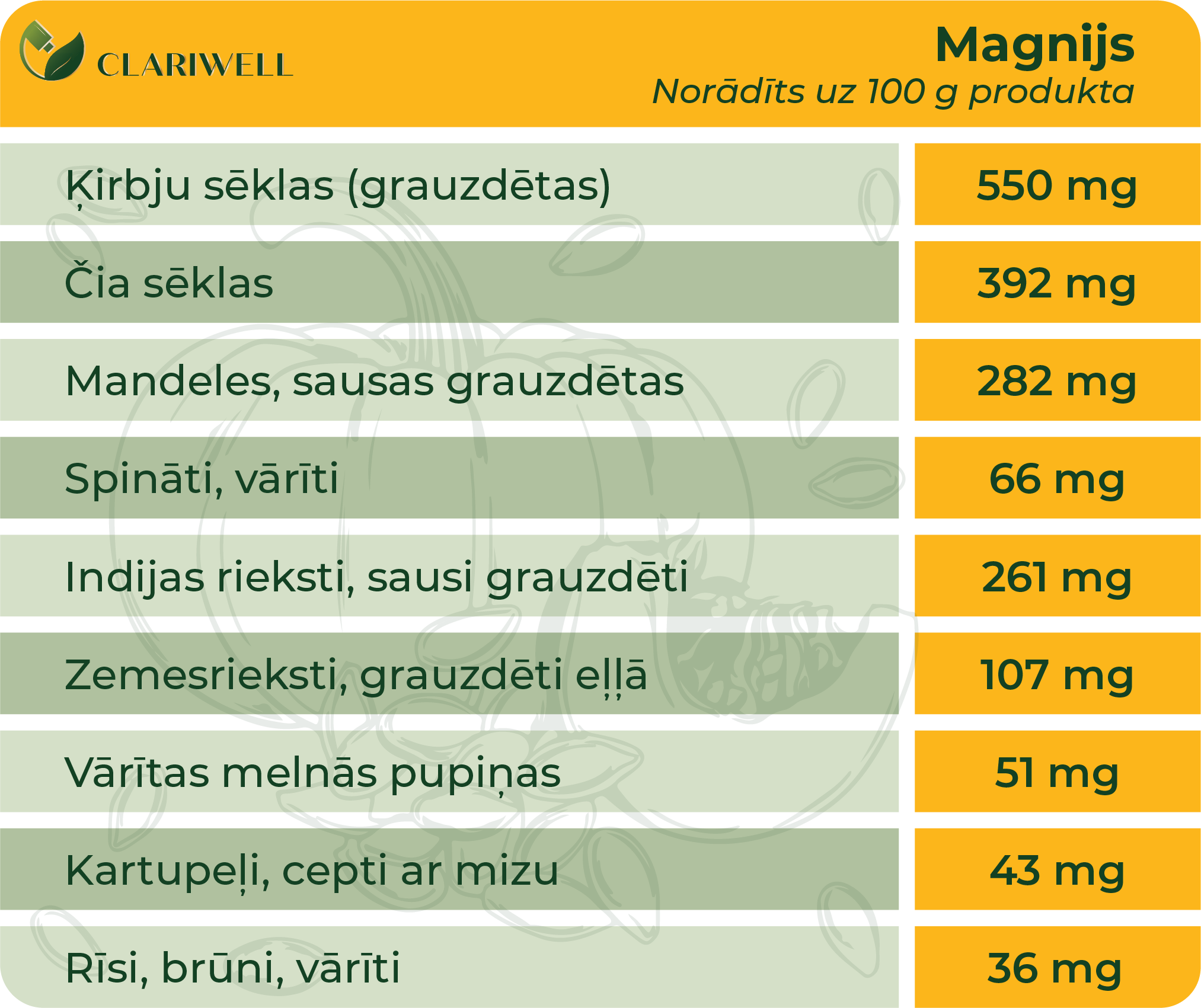
Vairums cilvēku var uzņemt pietiekami daudz magnija, ēdot tādus pārtikas produktus kā: zaļie lapu dārzeņi, sēklas (piemēram, ķirbju), veseli graudi, pupas, rieksti un zivis. Pieaugušiem cilvēkiem, kuriem nav novērots vai apstiprināts Magnija deficīts, normāli ir nepieciešams 350mg Magnija dienā.
Vairāki zāļu veidi var mijiedarboties ar magniju saturošiem uztura bagātinātājiem vai ietekmēt magnija stāvokli kopumā. Daži piemēri tiks minēti turpmāk. Cilvēkiem, kuri regulāri lieto šīs un citas šo grupu zāles, jāpārrunā magnija uzņemšana ar saviem veselības aprūpes sniedzējiem.
Bisfosfonāti
Uztura bagātinātāji ar augstu magnija saturu vai medikamenti var samazināt perorālo bisfosfonātu, piemēram, alendronāta (Fosamax®), ko lieto osteoporozes ārstēšanai, uzsūkšanos. Ar magniju bagātinātu pārtikas piedevu vai medikamentu un perorālo bifosfonātu lietošanā jāievēro vismaz 2 stundu intervāls.
Antibiotikas
Magnijs var veidot nešķīstošus kompleksus ar tetraciklīniem, piemēram, demeklociklīnu (Declomycin®) un doksiciklīnu (Vibramycin®), kā arī hinolonu grupas antibiotikām, piemēram, ciprofloksacīnu (Cipro®) un levofloksacīnu (Levaquin®). Šīs antibiotikas jālieto vismaz 2 stundas pirms magniju saturoša uztura bagātinātāja lietošanas vai 4–6 stundas pēc tā.
Diurētiskie līdzekļi
Hroniska ārstēšana ar cilpas diurētiskajiem līdzekļiem, piemēram, furosemīdu (Lasix®) un bumetanīdu (Bumex®), un tiazīdu grupas diurētiskajiem līdzekļiem, piemēram, hidrohlortiazīdu (Aquazide H®) un etakrīnskābi (Edecrin®), var pastiprināt magnija izdalīšanos ar urīnu un izraisīt magnija izsīkumu organismā. Turpretī kāliju aizturoši diurētiskie līdzekļi, piemēram, amilorīds (Midamor®) un spironolaktons (Aldactone®), samazina magnija izdalīšanos.
Protonu sūkņu inhibitori
Recepšu protonu sūkņa inhibitoru (PSI) zāļu, piemēram, ezomeprazola magnija (Nexium®) un lansoprazola (Prevacid®), ilgstoša lietošana (parasti vairāk nekā gadu) var izraisīt hipomagnezēmiju. ASV Pārtikas un zāļu pārvaldes izskatītajos gadījumos magnija piedevas bieži paaugstināja zemo magnija līmeni serumā, ko izraisīja PSI. Tomēr 25% gadījumu piedevas nepaaugstināja magnija līmeni, un pacientiem bija jāpārtrauc PSI lietošana. ASV Pārtikas un zāļu pārvalde iesaka veselības aprūpes speciālistiem apsvērt magnija līmeņa mērīšanu pacienta serumā pirms ilgstošas PSI terapijas uzsākšanas un periodiski pārbaudīt šo pacientu magnija līmeni. 1
Magnijs parasti ir labi panesams. Tomēr jāņem vērā, ka jebkuram magniju saturošam uztura bagātinātājam var būt arī magnija izraisītas blakus parādības. Lielākais magnija trūkums ir iespēja dažiem cilvēkiem izraisīt caureju, vieglus vēdera krampjus, kuņģa darbības traucējumus, sliktu dūšu, vemšanu un citas blakusparādības. Magnija saturoši produkti piesardzīgi jālieto cilvēkiem ar zemu asinsspiedienu, jo magnijs var to pazemināt.
Iespējams, ka magnijs ir viens no visvairāk pētītajiem minerāliem, tieši cilvēkiem ar migrēnu vai galvassāpēm. Atsevišķi pētījumi liecina, ka cilvēkiem ar migrēnu, magnija līmenis mēdz būt zemāks nekā cilvēkiem, kuriem nav galvassāpes. Daži zinātnieki uzskata, ka magnijs bloķē signālus smadzenēs, kas noved pie migrēnas ar auru vai redzes un citu maņu izmaiņām. Pētījumi arī liecina, ka magnijs aptur noteiktas ķīmiskas vielas, kas izraisa sāpes. Turklāt šķiet, ka magnija līmeņa pazemināšanās arī izraisa smadzeņu asinsvadu sašaurināšanos, kas potenciāli var sekmēt migrēnas rašanos.
Migrēna ir neiroloģisks traucējums, kuram raksturīgas izteiktas sāpes galvā un citi dažādi simptomi, piemēram, slikta dūša, vemšana, fotofobija, fonofobija un dažreiz redzes maņu traucējumi. Magnijs ir cilvēka ķermenim nepieciešams jons, un tam ir izšķiroša nozīme veselības un dzīves kvalitātes nodrošināšanā. Viena no galvenajām magnija lomām ir saglabāt neironu elektrisko potenciālu. Tāpēc magnija deficīts var izraisīt neiroloģiskas komplikācijas. Migrēna parasti ir saistīta ar zemu magnija daudzumu asins serumā un cerebrospinālajā šķidrumā. Magnija deficītam ir nozīmīga loma migrēnas patoģenēzē. Tieši tādēļ magnijs ir plaši izmantots migrēnas profilaksē un ārstēšanā .
Zinātniskajos pētījumos, kuros dalībnieki ik dienas saņēma papildus magniju migrēnas profilakses nolūkos, tika izmantotas dažādas magnija devas (no 400 mg līdz 1200 mg dienā) un tas tika lietots atšķirīgu laika periodu, tāpēc ir grūti precīzi noteikt, cik daudz magnija cilvēkam nepieciešams, lai novērstu migrēnu, un tas, visticamāk, ir individuāli (atkarībā no tā, cik smags ir konkrētā cilvēka magnija deficīts).
Taču ir dažas organizācijas, piemēram, Kanādas Galvassāpju biedrība, kas iesaka magniju kā profilaktisku migrēnas terapiju pieaugušajiem un konkrēti - īpašu magnija devu – 600 mg elementārā magnija dienā.
Ja ievērojat, ka magnija saturoši uztura bagātinātāji nepalīdz atvieglot jūsu migrēnas lēkmes, tas var būt divu būtisku iemeslu dēļ:
Jūsu lietotajam uztura bagātinātājam nav īpaši laba biopiejamība, proti, tas netiek labi absorbēts. Tas parasti notiek ar zemas kvalitātes uztura bagātinātājiem, kuros ir zema lietotā magnija elementārā vērtība (ne vienmēr norādītais magnija daudzums uztura bagātinātāja sastāvā nozīmē, ka tik daudz elementārā magnija satur produkts), kā arī atšķirīgiem magnija veidiem ir labāka vai sliktāka biopiejamība nekā citiem.
Ja pēc noteiktās diennakts devas lietošanas jums ir caureja, visticamāk, uztura bagātinātājs netiek absorbēts pietiekami labi un nesniedz vēlamo efektu.
Lai gan nav vispārpieņemtas definīcijas, stresu var skaidrot kāsarežģītas adaptīvas bioķīmiskas, fizioloģiskas, psiholoģiskas un gēnu ekspresijas izmaiņas organismā (stresa reakcija), ko izraisastimuls (stresors), un kuru smadzenes interpretē kā bīstamu.
Magnija satura līmenis organismā ir ļoti saistīts ar stresa līmeni, jo gan stress, gan hipomagnēmija (samazināts magnija daudzumsasinīs) pastiprina viens otra negatīvo ietekmi. Pastāvothipomagnēmijai, stresa rezultātā veidojas virkne traucējumu, kā,piemēram, gaismjutīgas galvassāpes, fibromialģija (traucējumi, kam raksturīgas plašas muskuļu un skeleta sistēmas sāpes, ko papildina nogurums, miegs, atmiņas traucējumi u.c.), hroniskanoguruma sindroms, audiogēnais stress, aukstuma stress un fiziskais stress.
Magnija pāreja no intracelulārās (šūnas iekšienē) uz ārpusšūnutelpu primāri nodrošina aizsargājošu lomu, lai mazinātu stresanelabvēlīgo ietekmi, bet ilgstoši stresa periodi izraisa progresējošumagnija deficītu un kaitīgas sekas veselībai.
Arvien vairāk pētījumu apliecina, ka psiholoģiskais stress veicinaoksidatīvo stresu, galvenokārt kateholamīnu autooksidācijas dēļ, kāarī psiholoģiskais stress pastiprina lipīdu peroksidāciju, palielinaDNS oksidatīvā bojājuma marķieru un samazina plazmasantioksidantu aktivitāti. Šeit būtiski, ka tieši magnijs antagonizē(pretdarbojas) daudzus no šiem procesiem.
- Vārds "magnijs" nāk no Grieķijas reģiona Magnēzijas, kurā atrodami šī elementa dabiskie savienojumi.
- Magnija piens, kas darbojas kā caurejas līdzeklis un ārstē gremošanas traucējumus, ir magnija, ūdeņraža un skābekļa molekulu savienojums.
- Nedzēsiet magnija liesmu ar ūdeni. Pēc degošā magnija apsmidzināšanas ar ūdeni, tas sāks degt vēl straujāk, ar smailu liesmu.
- Magnija jonu garša ir skāba un rūgta. Neliels magnija daudzums piešķir minerālūdenim garšu.
- Magnijs pēc masas daudzuma ir 11. visizplatītākais elements cilvēka ķermenī. Magnija joni ir atrodami katrā ķermeņa šūnā.
- Aptuveni 60% no cilvēka ķermeņa esošā magnija atrodas skeletā, 39% – muskuļu audos, un 1% atrodas ārpus šūnām.

Koenzīms Q10
Koenzīms Q10 ir taukos šķīstoša viela, ko izstrādā aknas. Neliels daudzums koenzīma Q10 tiek uzņemts arī ar pārtiku. Pēc savām īpašībām tas atgādina vitamīnus. Koenzīms Q10 piedalās enerģijas ražošanā un ir svarīgs antioksidants. Ja koenzīma Q10 līmenis organismā ir zems, tas var izraisīt daudzus neirodeģeneratīvus traucējumus.
Koenzīms Q10 (CoQ10) ir dzīvās šūnās dabiski sastopams komponents. Tas fizioloģiski darbojas kā spēcīgs antioksidants, membrānas stabilizators un kofaktors adenozīna trifosfāta (ATF) ražošanā oksidatīvās fosforilēšanas ceļā, kavējot proteīnu un DNS oksidēšanos. ATF ir nukleotīds ar ļoti lielu nozīmi dzīvo organismu vielmaiņā. Tas ir universāls enerģijas avots organismos noritošajiem bioķīmiskajiem procesiem. Attiecīgi CoQ10 ir svarīgs gan vielmaiņas, gan bioķīmiskajiem procesiem organismā.
CoQ10 pirmo reizi tika apstiprināts 1973. gadā Japānā kā zāles sirds mazspējas pacientu ārstēšanai, un to kā zāles lieto arī dažās citās valstīs. Tomēr vairumā valstu, piemēram, ASV un Eiropā, CoQ10 jau vairāk nekā 20 gadus tiek plaši izmantots kā pārtikas piedeva vai uztura bagātinātājs veselīga organisma stāvokļa uzturēšanai.
Bija zināms, ka CoQ10 jeb ubikvinonam ir noteicoša loma mitohondriju bioenerģētikā kā elektronu un protonu nesējam. Turpmākie pētījumi parādīja CoQ10 klātbūtni arī citās šūnu membrānās un asins plazmā, un pētījumu gaitā tika plaši izpētīta tā antioksidanta loma. Turklāt jaunākie dati liecina, ka CoQ10 ietekmē cilvēka šūnu signalizēšanā, metabolismā un transportēšanā iesaistīto gēnu ekspresiju. CoQ10 nepietiekamība ir saistīta ar autosomālām recesīvām mutācijām, mitohondriju slimībām, ar novecošanos saistītu oksidatīvo stresu un kanceroģenēzes procesiem, kā arī statīnu (lipīdu līmeni pazeminošu zāļu klase) terapijas sekundāro efektu. Ar zemu CoQ10 līmeni ir saistīti daudzi neirodeģeneratīvie traucējumi: diabēts, vēzis, fibromialģija, muskuļu, sirds un asinsvadu slimības.
Kaut arī lielākoties cilvēka organisms pats saražo visu nepieciešamo CoQ10 daudzumu, dažos gadījumos tomēr tā nenotiek. Ķermenī kopumā ir no 500 līdz 1500 miligramiem CoQ10, un ar gadiem tas samazinās.
Nav ideālās CoQ10 devas, jo ikviena cilvēka vajadzības atšķiras. CoQ10 standarta devas uztura bagātinātājos svārstās no 60 līdz 500 miligramiem dienā un augstākā ieteicamā dienas deva ir aptuveni 1200 miligrami. CoQ10 nepietiekamības iemesli var būt:
- Noteiktu vitamīnu, piemēram, B6 trūkums
- Mitohondriju slimības
- Ģenētiski defekti, kas ietekmē CoQ10 ražošanu
- Oksidatīvais stress vai brīvo radikāļu un antioksidantu disbalanss
Daži pārtikas produkti, kas satur CoQ10:
- Dzīvnieku iekšējo orgānu gaļa (sirds, aknas un nieres) satur visvairāk CoQ10 uz 100 gramiem.
- Treknas zivis, piemēram, foreles, makreles un sardīnes, satur CoQ10.
- Gaļa
- Sojas pupiņu produkti, piemēram, tofu, sojas piens un sojas jogurts, ir vērtīgs olbaltumvielu, kā arī CoQ10 avots cilvēkiem, kuri neēd gaļu.
- Dārzeņi un augļi – papildus dažādiem vitamīniem un minerālvielām daudzi dārzeņi un augļi satur CoQ10. Starp tiem jāpiemin brokoļi, spināti, avokado un upenes.
Pieaugušiem cilvēkiem, kuriem nav novērots vai apstiprināts CoQ10 deficīts, normāli ir nepieciešams 90-200mg CoQ10 dienā.
CoQ10 kā uztura bagātinātājs vai zāles ir izmantots vairāk nekā 30 gadus. Publicētie pirmsklīnisko un klīnisko drošuma pētījumu dati ir parādījuši, ka CoQ10 nerada nopietnas nevēlamas sekas cilvēkiem un to var droši lietot kā uztura bagātinātāju. Farmakokinētiskie pētījumi ar dzīvniekiem un cilvēkiem liecina, ka eksogēns CoQ10 neietekmē CoQ biosintēzi un neuzkrājas plazmā vai audos pēc papildus uzņemšanas pārtraukšanas.
CoQ10 ir viens no spēcīgākajiem antioksidantiem organismā, kas pie tam atjauno citus antioksidantus organismā un tam ir svarīga loma aizsardzībā pret reaktīvā skābekļa bojājumiem (reaktīvais skābeklis var iznīcināt cilvēka šūnas). CoQ10 ir vienīgais zināmais lipīdos šķīstošais antioksidants! Hroniskas migrēnas laikā veidojas iekaisuma procesi, kuri traucē papildināt antioksidantu krājumus, attiecīgi samazinot iespēju atbrīvoties no migrēnas diskomforta.
CoQ10 galvenokārt atrodas šūnu mitohondrijos un palīdz uzlabot šūnu darbību, tādējādi mazinot iekaisumu migrēnas laikā. Tā kā migrēna un iekaisums ir savstarpēji saistīti, CoQ10 varētu samazināt vai pat novērst migrēnas izraisītas galvassāpes.
Migrēnas fiziopatoloģija vēl nav pilnībā izprasta, taču asinsvadu un neironu disfunkciju var izskaidrot ar skābekļa apmaiņas traucējumiem, kas rodas mitohondriju disfunkcijas rezultātā. Attiecībā uz mitohondriju traucējumiem vismaz daļai migrēnas pacientu un, ņemot vērā nozīmīgo CoQ10 lomu mitohondriju enerģijas uzkrāšanā, CoQ10 varētu kalpot kā profilaktisks līdzeklis pret migrēnu.
- Taukos šķīstoša, vitamīniem līdzīga viela, kura galvenokārt rodas ķermeņa šūnu mitohondrijos.
- Rada 95% no visas cilvēka ķermeņa enerģijas.
- Ir sastopams gan dabīgs, gan sintētisks CoQ10; ubikvinonu ražo patentētas baktērijas; ubikvinolu ražo, fermentējot raugu.
- Sirds ir ievērojams orgāns, jo 24 stundu laikā tā sitas 100 000 reižu un līdz 70 gadu vecumam – 2,5 miljardus reižu bez nevienas brīvdienas. Tādēļ tā prasa milzīgu enerģijas daudzumu. Tieši šī iemesla dēļ, daba sirdī ir ievietojusi vairāk CoQ10 nekā citos orgānos.
- Pastāv uzskats, ka 50% pacientu ar lieko svaru ir zems CoQ10 līmenis. Vielmaiņas paātrināšana ar CoQ10 ir drošs veids, kā palīdzēt zaudēt svaru.
- Vairākos pētījumos ir secināts, ka, pateicoties antioksidantu aizsardzībai, papildus uzņemts CoQ10 var uzlabot spermas kvalitāti, aktivitāti un koncentrāciju.

Meiteņu zeltpīpenīte (Tanacetum parthenium L.)
Meiteņu zeltpīpenīte (Tanacetum parthenium L.) ir kumelītei līdzīgs daudzgadīgs lakstaugs ar izteiktu smaržu. Nav toksisks un to audzē kā dekoratīvu augu. Meiteņu zeltpīpenītei piemīt pretiekaisuma un dažādu sāpju atvieglojošas īpašības. Pētījumi uzrādījuši, ka meiteņu zeltpīpenīte ir īpaši efektīva migrēnas un galvassāpju gadījumā.
Meiteņu zeltpīpenīte (Tanacetum parthenium L.) ir daudzgadīgs kurvjziežu lakstaugs, kas vizuāli līdzinās margrietiņai un ir sastopams dārzos un ceļmalās. Šī auga nosaukums ir cēlies no latīņu vārda “febrifugia”, kas nozīmē “drudža mazinātājs”. Pirmajā gadsimtā dzīvojošais grieķu ārsts Dioskorīds ordinēja meiteņu zeltpīpenīti “visiem karstajiem iekaisumiem”. Pateicoties kuplajām lapām to dēvēja arī par “pūklapi”. Tas ir īss, krūmājam līdzīgs aromātisks daudzgadīgs augs, kas stiepjas 0,3 - 1 m augstumā. Dzeltenīgi zaļās lapas parasti ir īsākas par 8 cm, gandrīz bez matiņiem, plūksnaini dalītas (kā krizantēmai). Dzeltenie, 2 cm diametrā lielie ziedi uzplaukst jūlijā un noturas līdz pat oktobrim. Tie līdzinās kumelītei (Matricaria chamomilla), ar ko dažreiz tiek jaukta, un ziediņiem ir viena, uz ārpusi vērsta ziedlapiņu kārta, ziedi aug nelielos kurvīšos. Šis aromātiskais augs izdala spēcīgu un rūgtenu smaržu. Dzeltenīgi zaļās lapas ir izkārtotas pamīšus (proti, lapas aug abās kāta pusēs, bet ir izkārtotas pamīšus), klātas maziem matiņiem un ir nokarenas. Mazās, margrietiņām līdzīgās puķes veido blīvu ceru ar līdzenu augšpusi.
Meiteņu zeltpīpenīte (Tanacetum parthenium L.) ir ārstniecības augs, kas jau izsenis izmantots drudža, migrēnas izraisītu galvassāpju, reimatoīdā artrīta, vēdersāpju, zobu sāpju, kukaiņu kodumu, neauglības un menstruālā cikla traucējumu, kā arī dzemdību kontrakciju gadījumā. Meiteņu zeltpīpenīte kopš seniem laikiem ir lietota kā tradicionālajā, tā tautas medicīnā, un to bija īpaši iecienījuši grieķu un agrīnie Eiropas homeopāti. Meiteņu zeltpīpenīte ir tikusi izmantota, lai mazinātu psoriāzi, alerģijas, astmu, tinnītu, reiboni, sliktu dūšu un vemšanu. Augs satur daudz dabisku vielu, taču aktīvie mehānismi, visticamāk, ietver vienu vai vairākus sastāvā esošos seskviterpēna laktonus, tostarp partenolīdu. Citas iespējami aktīvās sastāvdaļas ir flavanoīdi – glikozīdi un pinēni. Augam piemīt vairākas dziednieciskās īpašības – pretvēža, pretiekaisuma, kardiotoniska, antispazmatiska, menstruācijas veicinoša, un to var izmantot prettārpu klizmās. Tas tiek plaši kultivēts dažādos pasaules reģionos un kā ārstniecības augs tas gūst aizvien vairāk panākumu, it sevišķi pateicoties vairākiem un pārliecinošākiem pierādījumiem par daudzveidīgo ārstniecisko ietekmi.
Par meiteņu zeltpīpenītes lietošanu nav saņemti nopietnu blakņu ziņojumi. Ir iespējamas šādas blaknes: slikta dūša, gremošanas problēmas un vēdera pūšanās; košļājot svaigas lapas, var rasties mutes gļotādas jēlumi un kairinājums.
Cilvēki, kas ir jutīgi pret ambrozijām un tām radniecīgiem augiem, var būt alerģiski arī pret meiteņu zeltpīpenītēm.
Meiteņu zeltpīpenīti nav ieteicams lietot grūtniecēm, jo tā var izraisīt dzemdes kontrakcijas. Šobrīd nav daudz datu par meiteņu zeltpīpenītes lietošanas ietekmi uz zīdīšanu.
Meiteņu zeltpīpenītes ārīga lietošana var izraisīt ādas kairinājumu.
Meiteņu zeltpīpenīte (Tanacetum parthenium L.) ir labi zināms augs, ko izmanto migrēnas profilaksē.
Meiteņu zeltpīpenīte ir ārstniecības augs, kura ārstniecisko īpašību potenciāls un ievērojamā spēja mazināt galvassāpes bija atzīta pat viduslaikos. Meiteņu zeltpīpenītes ārstnieciskā ietekme migrēnas patofizioloģijā vēl nav līdz galam izprasta. Meiteņu zeltpīpenītes ekstrakts veicina serotonīna (5-hidroksitriptamīna) izdalīšanos no trombocītiem, ko nodrošina vairāki agregācijas mediatori. Fizioloģiski serotonīns iesaistās nervu impulsu pārvadē starp nervu šūnām. To sauc par neirotransmiteru. Serotonīnu galvenokārt atrod smadzenēs, kuņģa-zarnu traktā un trombocītos. Serotonīna darbība cilvēka organismā īpaši ir saistīta ar gludās muskulatūras aktivitāti un impulsu pārraidi starp nervu šūnām, turklāt tā veidošanās ierosina laimes izjūtu un labsajūtu.
Meiteņu zeltpīpenītes ekstrakti un tīrs partenolīds nomāc prostaglandīnu sintēzi. Tā kā prostaglandīni ir vielas, kas izraisa iekaisumu, sāpes, eksudāta (šķidruma, kas izplūst no asinsvadiem iekaisuma laikā) veidošanos un drudzi, tad meiteņu zeltpīpenīte spēj labvēlīgi iedarboties, novēršot vai mazinot šīs parādības. Partenolīds, savukārt, būtiski ietekmē asinsvadu sašaurināšanās un paplašināšanās mehānismus.
Vairāki klīniskie pētījumi ir apliecinājuši, ka meiteņu zeltpīpenītes ieguvumi migrēnas profilaksē krietni pārsniedz riskus. Attiecībā uz meiteņu zeltpīpenītes drošumu un panesamību klīniskajos pētījumos un no ilgstošu lietotāju ziņojumiem nav gūtas liecības par nopietnām blaknēm.
Meiteņu zeltpīpenītes ekstrakti nomāc trombocītu 5-HT sekrēciju, neitralizējot sulfhidril grupas gan šūnā, gan ārpus tās. Meiteņu zeltpīpenītē esošie seskviterpēni satur alfametilēnbutirolacetona vienības, kas spēj reaģēt ar sulfhidril grupām.
Meiteņu zeltpīpenītei, šķiet, ir vairāk nekā viens iedarbības mehānisms. Auga ekstrakti ietekmē ļoti daudzus fizioloģiskos iedarbības ceļus. Dažus no šiem mehānismiem jau aplūkoti iepriekš, piemēram, prostaglandīna sintēzes nomākšanu, asinsvadu gludo muskuļu spazmu samazināšanu un trombocītu granulu sekrēcijas bloķēšanu.
Meiteņu zeltpīpenīte ir pazīsatama visā pasaulē, piemēram, Kanādas Veselības aizsardzības nodaļa ir piešķīrusi zāļu identifikācijas numuru (ZIN) meiteņu zeltpīpenītes produktam, ļaujot tā ražotājam apgalvot, ka šis bezrecepšu medikaments novērš migrēnas izraisītas galvassāpes.
Arī Eiropā meiteņu zeltpīpenīte ir plaši pētīta un Eiropas zāļu aģentūras novērtējuma ziņojumā par meiteņu zeltpīpenīti (EMA/HMPC/48716/2019) ir secināts, ka meiteņu zeltpīpenīte tiek izmantota migrēnas un galvassāpju novēršanai ar terapeitisko devu 100 mg drogu dienā.
- Senie grieķi šo augu dēvēja par “Parthenium”, visticamāk, tādēļ, ka to 5. gs. pr. Kr. izmantoja kā ārstniecības līdzekli, lai glābtu dzīvību no Partenona nokritušajiem tā būvniecības laikā.
- Vēl viens meiteņu zeltpīpenītes nosaukums ir “viduslaiku aspirīns” jeb 18. gadsimta “aspirīns”.
- Centrālamerikā un Dienvidamerikā šo augu izmantoja daudzu kaišu ārstēšanai. Andu kalnos dzīvojošie Kalovejas indiāņi šo vērtīgo augu izmanto koliku, sāpīgu nieru, rīta nelabuma un vēdersāpju ārstēšanai. Kostarikāņi izmanto auga novārījumu, lai uzlabotu gremošanu, kā kardiotonisku un menstruācijas veicinošu līdzekli un kā prettārpu klizmu. Meksikā to izmanto kā antispazmatisku un tonizējošu līdzekli, kas regulē menstruālo ciklu. Venecuēlā ar to ārstēja ausu sāpes
- Meiteņu zeltpīpenīti mēdz stādīt ap mājām kā gaisa attīrītāju, jo tai piemīt spēcīgs, paliekošs aromāts, un tās ziedu tinktūra tiek izmantota kā kukaiņu atbaidītājs un uz kodumiem klājams balzams. Tas ir ticis izmantots kā pretinde pārmērīgas opija lietošanas gadījumā.

Vitamīns B2 (Riboflavīns)
Vitamīns B2 jeb Riboflavīns ir ūdenī šķīstošs vitamīns, kas ietilpst fermentu sistēmās piedaloties audu elpošanas, ogļhidrātu un olbaltumvielu šķelšanas nodrošināšanā. Tas ir nepieciešams, lai pareizi funkcionētu gremošanas trakts, asins šūnas un smadzeņu darbība. Riboflavīna galvenie pētījumu virzieni ir saistīti ar tā ietekmi uz audzējiem un migrēnas tipa galvassāpēm.
1872. gadā Blaits atklāja riboflavīnu kā dzeltenu fluorescējošu pigmentu pienā, bet šī pigmenta vitamīna īpašība tika noteikta tikai 1930-to gadu sākumā. Augi un daži mikroorganismi spēj sintezēt riboflavīnu, tomēr tā ir cilvēka veselībai būtiska barības viela, kas jānodrošina ar uzturu.
Riboflavīns jeb B2 vitamīns, ir karstumizturīgs, ūdenī šķīstošs vitamīns, ko organisms izmanto, lai enerģijas ieguvei ogļhidrātus, taukus un olbaltumvielas metabolizētu glikozē. Tas ne tikai spēj palielināt enerģijas līmeni, bet arī darbojas kā antioksidants un nodrošina pareizu imūnsistēmas, veselīgas ādas un matu folikulu darbību. Šāda iedarbība rodas ar divu koenzīmu, flavīna mononukleotīda (FMN) un flavīna adenīna dinukleotīda (FAD) palīdzību. Riboflavīna deficīta gadījumā organisms nespēj pārstrādāt tādus makroelementus kā, piemēram, taukus, ogļhidrātus un olbaltumvielas, kas nepieciešami ķermeņa uzturēšanai. Riboflavīns ir nepieciešams normālai organisma attīstībai, laktācijai, fiziskai veiktspējai un reproduktīvajai sistēmai.
Ja cilvēka gremošanas sistēma ir vesela, organisms lielāko daļu uzturvielu var uzņemt no pārtikas, tāpēc ir svarīgi, lai ikdienas pārtika saturētu to atbilstošā daudzumā. Kā jau minējām, riboflavīnam ir dzeltenzaļš fluorescējošs pigments, kas piešķir urīnam dzeltenu nokrāsu, norādot, ka ķermenis absorbē riboflavīnu. Riboflavīns arī palīdz pārvērst triptofānu par niacīnu, kas savukārt aktivizē B6 vitamīnu.
Riboflavīna deficītu var izraisīt nepietiekama barības vielu uzņemšana vai endokrīnās sistēmas patoloģijas. Riboflavīna deficīts korelē arī ar citu B kompleksa vitamīnu trūkumu. Tas dabiski ir sastopams tādos pārtikas produktos kā olas, piena produkti, gaļa, zaļie dārzeņi un graudi. Antioksidants riboflavīns darbojas pēc tāda paša principa kā glutations. Glutations ir organisma antioksidants – vienkāršs peptīds, kas sastāv no trīs aminoskābēm – glicīna, cisteīna un glutamīna. Tam piemīt vairākas dzīvībai svarīgas īpašības, kas regulē organisma procesus – stiprina imunitāti, ražo enerģiju, aizkavē šūnu novecošanos, pazemina holesterīna līmeni. Ikviena organisma šūna ražo glutationu, taču ikdienā tā rašanos samazina un aizkavē neskaitāmi faktori, piemēram, nepilnvērtīgs uzturs, medikamentu lietošana, stress, infekcijas. Glutationa darbība ir vērsta uz brīvo radikāļu neitreizēšanu un aknu atindēšanu, jo brīvie radikāļi var veicināt vairāku slimību attīstību. Riboflavīna deficīta cēlonis var būt arī hroniska caureja, aknu darbības traucējumi, alkoholisms un hemodialīze.
Kā Riboflavīna nepietiekamības riska grupas var minēt:
Sportisti. Slodze rada vielmaiņai stresu, kura laikā tiek pastiprināti izmantots riboflavīns.
Grūtnieces un sievietes, kuras baro ar krūti (reizēm arī zīdaiņi). Grūtniecēm vai sievietēm zīdīšanas laikā, kuras reti lieto gaļu vai piena produktus, draud riboflavīna deficīts, kas var nelabvēlīgi ietekmēt gan māmiņu, gan zīdaiņu veselību. Piemēram, riboflavīna deficīts grūtniecības laikā var palielināt preeklampsijas risku.
Cilvēki, kuri ir veģetārieši vai vegāni un/vai patērē maz piena. Tiem, kas ēd gaļu un piena produktus, šie pārtikas produkti nodrošina ievērojamu devu riboflavīna. Tādēļ cilvēkiem, kuri dzīvo jaunattīstības valstīs un kuriem gaļa un/vai piena produkti ir pieejami ierobežotā daudzumā, ir palielināts riboflavīna deficīta risks. Arī veģetāriešiem un vegāniem un tiem, kas attīstītajās valstīs patērē maz piena produktu, pastāv riboflavīna nepietiekamības risks.
Pieaugušiem cilvēkiem, kuriem nav novērots vai apstiprināts vitamīna B2 deficīts, normāli ir nepieciešams 1,3 mg vīriešiem, 1,1 mg sievietēm un 1,4 mg grūtnecēm vitamīna B2 dienā.
Situācijās, kad nepieciešama riboflavīna papildus uzņemšana, piemērotais daudzums var būt piecas līdz desmit reizes lielāks par dienas ieteicamo devu (1,3 mg vīriešiem, 1,1 mg sievietēm un 1,4 mg grūtniecības laikā). Līdz šim nav ziņots par toksisku vai nelabvēlīgu ietekmi, cilvēkiem lietojot lielas riboflavīna devas. Tomēr jāpieņem, ka liela riboflavīna deva var izraisīt antioksidantu līdzsvara traucējumus cilvēka organismā. Taču šajā jomā nav pārliecinošu pierādījumu un ir ieteicams veikt papildu pētījumus, lai noskaidrotu iespējamo negatīvo ietekmi no riboflavīna lietošanas lielos daudzumos.
Alerģiska reakcija pret šo vitamīnu ir novērojama reti. Tomēr nekavējoties sazinieties ar ārstu, ja pamanāt nopietnas alerģiskas reakcijas simptomus, tostarp: izsitumus, niezi/pietūkumu (īpaši sejas/mēles/rīkles), galvas reiboni, apgrūtinātu elpošanu. Taču šis nav pilns iespējamo blakusparādību saraksts.
Migrēnas galvassāpes parasti izraisa intensīvas pulsējošas vai durošas sāpes vienā galvas zonā. Dažreiz tās pavada aura (pārejoši fokālie neiroloģiskie simptomi pirms galvassāpēm vai to laikā). Dažu migrēnas veidu gadījumā par cēloņsakarīgu tiek uzskatīta mitohondriju disfunkcija. Tā kā mitohondriju funkcijai ir nepieciešams riboflavīns, pētnieki pēta riboflavīna lietošanu kā iespēju novērst vai ārstēt migrēnas galvassāpes.
Ir veikti dažādi pētījumi, kuros izmantots riboflavīns kā migrēnas profilakses vai ārstēšanas līdzeklis. Vairākos no šiem pētījumiem ir lietotas lielas riboflavīna devas – 400 mg un vairāk/dienā, taču atsevišķi pētījumi ir pierādījuši, ka nav nemaz nepieciešamas lielas riboflavīna ikdienas devas. Uzlabojumi ir novērojami jau pie 25 mg dienā, tiesa lietojot 3 mēnešus.
Kopumā pētījumi parāda, ka B2 vitamīna lietošana pieaugušajiem var pozitīvi ietekmēt migrēnas lēkmju biežuma un ilguma samazināšanu bez nopietnām blakusparādībām. Secinājums: šķiet, ka riboflavīns ir drošs un labi panesams risinājums migrēnas simptomu profilaksei pieaugušajiem.
- Pakļaujot riboflavīnu gaismai, tas viegli inaktivējas. Piens, kas tiek uzglabāts stikla tarā un ir pakļauts gaismai, zaudē lielu daļu riboflavīna satura. Necaurspīdīgas plastmasas pudeles un kartona tetrapakas aizsargā pienā esošo riboflavīnu. Gatavošanas laikā tiek zaudēts tikai neliels daudzums riboflavīna.
- No visiem B grupas vitamīniem riboflavīns ir, iespējams, visvieglāk saprotamais. Tas nozīmē, ka varat fiziski sajust, vai jūsu ķermeņa riboflavīna patēriņš ir bijis pietiekami liels, jo pamanīsiet, ka intensīva patēriņa laikā jūsu urīns būs izteikti dzeltens. Tas faktiski ir vienīgais vitamīns, kas sniedz uzskatāmu norādi par tā darbību jūsu ķermenī! Tā kā riboflavīns ir ūdenī šķīstošs vitamīns, jūsu ķermenis to katru dienu izskalo, tāpēc tas katru dienu jāuzņem no jauna.
- Lai ražotu B2 vitamīnu uztura bagātinātājiem vai pievienotu to pārtikai, rūpniecības uzņēmumi audzē īpašus raugus, sēnītes vai baktērijas, kas sintezē daudz riboflavīna.
- Riboflavīnam ir dzeltena vai oranžīgi dzeltena krāsa, tāpēc to var izmantot arī kā pārtikas krāsvielu. UV gaismā riboflavīns spīd spilgti zaļā krāsā.
- Svara zudums palielina nepieciešamību pēc riboflavīna par 60%. Vairāk nekā 20 minūtes kardio treniņa 6 dienas nedēļā arī palielina organisma vajadzību pēc riboflavīna par gandrīz 60%.

Holīns
Holīns jeb vitamīns B4 ir ļoti svarīgs elements smadzeņu un nervu sistēmas darbībai. Tas iekļaujas neirotransmiteru sastāvā, kas nodrošina nervu šūnu savstarpēju saziņu. Izpētīts, ka cilvēkiem, kuri uzņem pietiekami daudz holīna, ir labāka atmiņa un asāka domāšana. Organisms lielāko daļu holīna uzņem ar barību un nelielu daudzumu spēj izstrādāt aknās.
Holīns ir B grupas vitamīniem līdzīga uzturviela. To spēj sintezēt aknas. Tas ir sastopams arī tādos produktos kā gaļa, zivis, rieksti, pupas, dārzeņi un olas.
Holīns ir daudzām vielmaiņas reakcijām nepieciešamo metilgrupu avots. Organismam holīns ir vajadzīgs, lai sintezētu fosfatidilholīnu un sfingomielīnu – divus šūnu apvalkiem svarīgus fosfolipīdus. Tādēļ holīns ir nepieciešams visām augu un dzīvnieku šūnām, lai saglabātu to strukturālo veselumu.
Holīns piedalās daudzos organismam svarīgos procesos.
- Šūnu struktūrā. Tas ir vajadzīgs, lai sintezētu taukus, kas veido šūnapvalku viengabalainību.
- Šūnu komunikācija. Tas ir iesaistīts šūnu signālvielu sintēzē.
- Tauku transports un vielmaiņa. Tam ir svarīga loma tādu vielu sintēzē, kas ir nepieciešamas holesterīna aiznešanai no aknām. Nepietiekams holīna daudzums novedīs pie pārmērīgas tauku un holesterīna uzkrāšanās aknās.
- DNS sintēze. Holīns un citi vitamīni, piemēram, B12 un folskābe, veicina DNS sintēzei svarīgu procesu norisi.
- Vesela nervu sistēma. Šī uzturviela ir nepieciešama svarīga neirotransmitera – acetilholīna – sintēzei. Tas ir iesaistīts atmiņas darbībā, muskuļu kustības, sirdsdarbības un citu pamatfunkciju nodrošināšanā.
Cilvēka organisms spēj sintezēt holīnu aknā, galvenokārt fosfatidilholīna formā, taču daudzums, ko tas dabiski sintezē, nav pietiekams organisma patēriņa vajadzībām. Ierastākie holīna avoti pārtikā ir taukos šķīstoši fosfolipīdi – fosfatidilholīns un sfingomielīns – kā arī ūdenī šķīstošās vielas fosfoholīns, glicerolfosfoholīns un brīvais holīns. Apēdot holīnu saturošus savienojumus, aizkuņģa dziedzera un gļotādu izdalītie enzīmi atbrīvo brīvo holīnu no apmēram puses taukos šķīstošo formu un nedaudz no ūdenī šķīstošajām formām.
Citikolīnu veido divas molekulas: citidīns un holīns. Pastāv uzskats, ka citikolīns pavairo smadzenēm svarīgu ķīmisku vielu – fosfatidilholīnu. Šī ķīmiskā viela ir būtiska smadzeņu darbībai. Citikolīns var arī palielināt citu ķīmisko vielu, kas smadzenēs nodrošina komunikāciju, daudzumu. Citikolīnam un tā hidrolīzes produktiem (citidīnam un holīnam) ir svarīga loma fosfolipīdu veidošanā, kas iesaistīti šūnu membrānu veidošanā un atjaunošanā. Tie veicina arī tādas būtiskas vielmaiņas funkcijas kā nukleīnskābju, olbaltumvielu un acetilholīna veidošanos, kur acetilholīna ietekmē palēninās sirdsdarbība, paplašinās perifēriskie asinsvadi un pazeminās arteriālais spiediens, sašaurinās bronhi, pastiprinās peristaltika un gremošanas trakta dziedzeru sekretoriskā darbība. Acetilholīns piedalās atmiņas uzlabošanā un darbojas pretēji adrenalīnam.
Holīna trūkums organismā var izraisīt muskuļu bojājumu, aknu bojājumus un nealkoholisko taukaino aknu slimību (NTAS jeb hepatosteatozi) Holīna deficīts veseliem cilvēkiem, un sievietēm, kam nav grūtniecība, ir novērojams ļoti reti, iespējams, tādēļ, ka organisms to spēj sintezēt pats.
Lai gan ir sastopams ne pārāk plašs uzskats, ka veģetāriešiem un vegāniem pastāv augstāks holīna deficīta risks, tomēr tam nav viennozīmīgu pierādījumu.
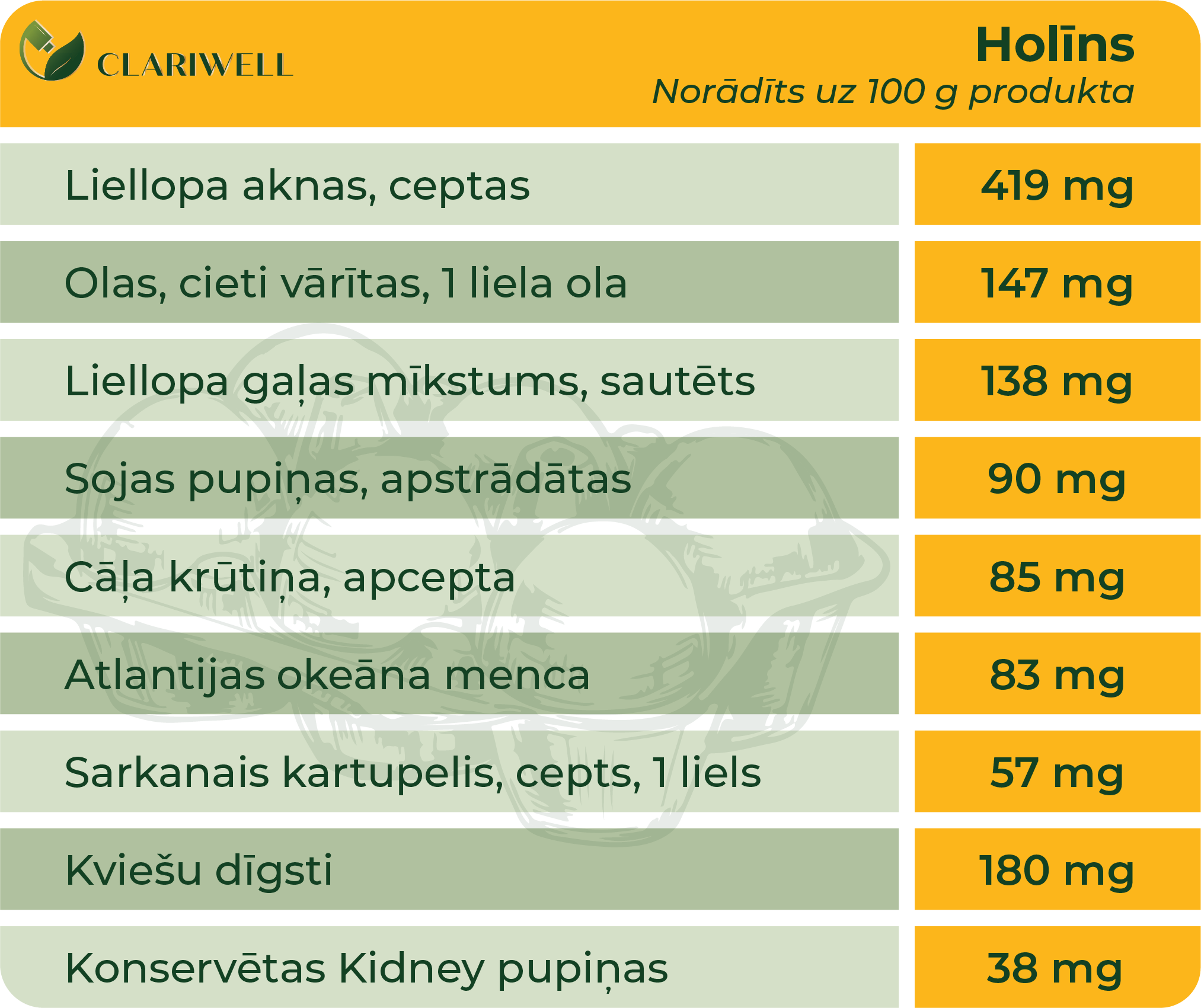
Patiesībā daži no produktiem, kam ir vislielākais holīna saturs, ir sojas pupiņas, kartupeļi un sēnes. Lai novērstu šādu deficītu, parasti pietiek ar uzturvielām bagātu diētu, kurā iekļauti nerafinēti produkti.
Pieaugušiem cilvēkiem, kuriem nav novērots vai apstiprināts holīna deficīts, normāli ir nepieciešams 550 mg vīriešiem un 425 mg sievietēm holīna dienā
Nav zināms par klīniski svarīgu holīna mijiedarbību ar citiem medikamentiem.
Insults ir postošs neiroloģiskais traucējums un trešais biežākais nāves cēlonis. Parasti insults rada smagu invaliditāti, augstu insulta atkārtošanās risku un citus nevēlamus iznākumus. Asins plūsmas trūkums vai samazinājums išēmiskā insulta ietekmē izraisa iekšējas novirzes orgānu un sistēmu darbībā, kas rada nervu šūnu bojājumus.
Neironu nāves iemesli gan novecošanās gadījumā, gan progresīvu neirona struktūras un funkciju zuduma slimību gadījumā - akūtā un hroniskā - ir vieni un tie paši. Tie ir kalcija jonu un brīvo radikāļu pārmērīga uzkrāšanās šūnā, oksidatīvais stress (tas rodas, ja organismā izveidojas pārāk daudz brīvo radikāļu - aktīvu molekulu, kuras ir iesaistītas daudzos procesos, kas kaitē veselībai un pakāpeniski paātrina novecošanos), mitohondriālā disfunkcija un metaboliskie traucējumi, kas rada acidozi (acidoze samazina sirds muskulatūras darbaspējas, izraisa asinsvadu spazmas, pasliktina audu apgādi ar skābekli. Acidozes ietekmē rodas elpošanas ritma traucējumi, apziņas traucējumi, pasliktinās smadzeņu un nieru asinsapgāde). Rezultātā šūnas signalizācijas mehānismi, kas ietver sevī tūkstošiem dažādu molekulu savstarpēju saistību, regulējot procesus no membrānas līdz kodolam un atpakaļ, ir pilnībā traucēti. Savukārt, šūna, kas gājusi bojā, nespēj ne saņemt, ne tālāk pārraidīt, ne saglabāt informāciju, līdz ar to cilvēka kognitīvajās (prāta) funkcijās rodas neirodeficīts.
Citidīna-5-difosfoholīns (citikolīns jeb CDP-holīns) ir fosfatidilholīna biosintēzes starpniekviela, kas apliecinājusi savu labvēlīgo ietekmi vairākos centrālās nervu sistēmas traumu gadījumos, tostarp novērojumos par smadzeņu išēmiju. Citikolīnu veido divas molekulas: citidīns un holīns. Citidīns un holīns katrs atsevišķi spēj šķērsot asins-smadzeņu barjeru, iekļūt smadzeņu šūnās un kalpot par CDP-holīna starpšūnu sintēzes izejmateriālu.
Citikolīns var:
- samazināt brīvo taukskābju atbrīvošanu (pārmērīgs brīvo taukskābju daudzums samazina insulīna jutību jeb izraisa insulīna rezistenci audos (aknu, sirds, muskuļu un taukaudos));
- atjaunot mitohondriju adenozīna trifosfatāzi (ATF) (nukleotīds ar ļoti lielu nozīmi dzīvo organismu vielmaiņā un tas ir universāls enerģijas avots organismos noritošajiem bioķīmiskajiem procesiem);
- tikt efektīvi izmantots smadzeņu šūnās membrānas lipīdu sintēzei, kur tas ne tikai palielina fosfolipīdu sintēzi, bet arī kavē fosfolipīdu noārdīšanos;
- samazināt vai novērst išēmijas un/vai hipoksijas ietekmi;
- samazināt un ierobežot nervu šūnu membrānas bojājumus, atjaunot intracelulāro regulējošo enzīmu jutīgumu un funkciju un ierobežot tūsku;
- veicināt uzmanības, mācīšanās un atmiņas veiktspējas uzlabošanos.
Citikolīns ne tikai veicina nukleīnskābju, proteīnu, acetilholīna un citu neirotransmiteru (bioloģiski aktīvas vielas, kas sintezējas neironā un izdalās sinapsē, saistoties ar citas šūnas receptoriem un pārnes nervu impulsu no sinapses uz šūnu) sintēzi, bet arī samazina brīvo radikāļu veidošanos, apstiprinot uzskatu, ka citikolīns vienlaikus kavē dažādu išēmisko kaskāžu soļus, pasargājot traumētos audus no agrīniem vai kavētiem mehānismiem, kas ir saistīti ar išēmiskajiem smadzeņu bojājumiem. Visbeidzot jāpiebilst, ka citikolīns var veicināt atveseļošanos, sekmējot sinapšu augšanu un palielinot neiroplastiskumu, vienlaikus samazinot neiroloģisko deficītu un uzlabojumus uzvedībā, spējā mācīties un atmiņas darbībā.
- Ne visi holīna avoti ir vienādi un ne vairāk par 50% no pārtikas uzņemtā holīna spēj sagremot zarnās mītošās baktērijas.
- Holīns nav vitamīns šī vārda striktā izpratnē, bet gan būtisks pārtikas amīns. Taču literatūrā to klasificē kā B4 vitamīnu.
- Holīna hidroksīda otrs nosaukums ir holīna bāze. Tas ir higroskopisks (mitrumu uzsūcošs) un līdz ar to bieži vien bezkrāsains, viskozs, hidratēts sīrups, kas smaržo kā timetilamīns (TMA). Holīna šķīdums ūdenī ir stabils, taču savienojums lēnām sabrūk un pārveidojas par etilēnglikolu, polietilēnglikolu un TMA.
- 1849. gadā Ādolfs Strekers kļuva par pirmo, kam izdevās holīnu izdalīt no cūkas žults. 1852. gadā L. Babo un M. Hiršbrunns ieguva holīnu no balto sinepju sēklām un nodēvēja par sinkalīnu. 1862. gadā Strekers atkārtoja eksperimentu ar cūkas un vērša žulti, nodēvējot vielu par “holīnu”, darinot nosaukumu pēc grieķu “holē”, kas nozīmē “žults”, un piešķirot tai ķīmisko formulu C5H13NO. 1850. gadā Teodors Nikolass Goblejs to ieguva no smadzenēm un karpu ikriem, un šo vielu nodēvēja par lecitīnu, atvasinot no grieķu “lekithos”, kas apzīmē olas dzeltenumu, un 1874. gadā pierādot, ka tā ir fosfatidilholīnu kombinācija.
- 1930. gadu sākumā Čārlzs Bests ar kolēģiem pamanīja, ka īpašu diētu ievērojošo žurku un ar diabētu sirgstošu suņu taukaino aknu var izārstēt, dodot viņiem lecitīnu, un 1932. gadā pierādot, ka šo funkciju paveic tieši lecitīnā esošais holīns.

Gotu kola (Centella asiatica L.)
Gotu kola (Centella asiatica L.) ir daudzgadīgs augs, kurš plaši izplatīts pasaules tropu un subtropu apgabalos. Āzijā uzskata, ka Gotu kola var pagarināt cilvēka dzīvi. Ājurvēdas medicīnā to uzskata par nervu un smadzeņu šūnu darbības izteiktu stiprinātāju un stimulantu. Gotu kola ir viens no parasti izmantotajiem augiem pēcinsulta stāvokļos. Tā ir iekļauta Indijas un Lielbritānijas farmaceitiskajā sistēmā (farmakopejā).
Gotu kola jeb vairoglape ir daudzgadīgs augs, kas pārsvarā sastopams Indijā, Japānā, Ķīnā, Indonēzijā, Dienvidāfrikā, Šrilankā un Klusā okeāna Dienvidu krastā. Tā pieder pie čemurziežu dzimtas un tai nav nedz izteiktas garšas, nedz smaržas. Tai ir vairāki nosaukumi – gotu kola, vairoglape, Āzijas vairoglape.
Šis augs ir iecienījis ūdens tuvumu. Tam ir nelielas, vēdeklim līdzīgas lapas un balti līdz mēļi vai sārti ziedi, un mazi, ovāli augļi. Gotu kolas lapas un kāti tiek izmantoti kā zāles. Šis augs var izplatīties nekontrolēti kā nezāle, taču tas ir atkarīgs no atrašanās vietas. Piemēram, seklā ūdenī lapas peld pa virsu, savukārt sausās teritorijās šim augam attīstās daudz sakņu un lapas drīzāk ir šauras un mazas. Vēdekļa formas lapas var būt gan gludas, gan daivveidīgas. Sarkanie ziedi pārtop par augli ar apmēram 5 mm diametru.
Vairoglapes galvenās aktīvās sastāvdaļas ir triterpenoīdi, taču jāņem vērā arī tas, ka no Indijas, Šrilankas un Madagaskaras nākušajiem augiem nebūs pilnīgi vienādas īpašības. Gotu kolas triterpēnu koncentrācija svārstās no 1,1 līdz 8%, un vairumam augu tā ir diapazona vidusdaļā.
Šis augs uzlabo mikrocirkulāciju galvā un perifērajā daļā, un tiek uzskatīts, ka tas uzlabo atmiņu. 1880. gados francūži iekļāva gotu kolu farmaceitisko līdzekļu klāstā.
Normālos apstākļos vairoglape ir veselībai droša. Taču ir piefiksētas arī dažas blaknes, ko radījis šis augs, piemēram, miegainība, slikta dūša, galvassāpes, reibonis, caureja, ādas kairinājums.
Lai gan nav veikti plaši pētījumi par gotu kolas iedarbību uz citiem medikamentiem, pastāv iespēja, ka tā var reaģēt uz recepšu vai bezrecepšu medikamentiem. Pirms gotu kolas lietošanas vienmēr konsultējieties ar ārstu.
Insults var izraisīt mentālo spēju samazināšanos. Kognitīvo spēju traucējumi pēc išēmiskā insulta ir raksturīgi 20 līdz 30% gadījumu, un to iespējamība palielinās divu gadu laikā pēc insulta. Ballard u.c. savā pētījumā konstatēja, ka 25% pacientiem ir pēcinsulta demence un insultu pārcietušajiem turpmākos piecus gadus ir deviņas reizes lielāks risks ciest no demences, nekā veseliem cilvēkiem, it īpaši izziņas spēju un ar tām saistīto funkciju – atmiņas un uzmanības – ziņā. Kognitīvo spēju traucējumus pēc smadzeņu asinsvadu slimībām vajadzētu pārvaldīt tā, lai novērstu insulta atkārtošanos un īpaši pievērstos izziņas spēju uzlabošanai. Sekundārā insulta profilakse paredz tādu riska faktoru kontroli kā asinsspiediens, holesterīna līmenis un hiperhomocistenēmija.
Viens no parasti izmantotajiem augu valsts līdzekļiem ir vairoglape jeb gotu kola. Galvenā substanču grupa gotu kolā ir triterpēni, tostarp aziatikozīds, madekasodīds, aziātskābe un madekānskābe, kam piemīt antioksidantu, pretiekaisuma un šūnu bojāeju novērsošas īpašības. Tas varētu skaidrot, kādēļ gotu kola pozitīvi ietekmē smadzeņu plastiskumu, kā arī pagarina dendrītus (nervu šūnu izaugumus). Eksperimentos ar pelēm tika secināts, ka šis augs pastiprina hipokampa CA3 neironu dentrītu sazarošanos, ja tos skārušas neirodeģeneratīvas slimības un atmiņas traucējumi.
Šis pētījums tika veikts, lai noteiktu pacientu ar asinsvadu bojājumu izraisītiem kognitīvās funkcijas traucējumiem uzlabojumu, novērtējot pēc Monreālas kognitīvā novērtējuma testa Indonēzijas varianta (MoCA-Ina) pēc 750 mg/dienā gotu kolas (centella asiatica) un 3 mg/dienā folskābes lietošanas 6 nedēļu periodā.
- Vēsturiski gotu kola ir izmantota sifilisa, hepatīta, kuņģa čūlu, prāta noguruma, epilepsijas, caurejas, drudža un astmas ārstēšanā.
- Eiropā kādreiz valdīja maldīgs uzskats, ka vairoglape izraisa aitu nagu eroziju.
- Indijā vairoglape tiek uzskatīta par augu ar ļoti spēcīgu iedarbību uz cilvēka garīgajām spējām, Ajurvēdas medicīna to sauc par Brahmi, jo tā palīdz iegūt zināšanas par garīgumu.
- Klīst leģenda, ka ķīniešu homeopāts Lī Činjuns dzēra augu mikstūru, kuras sastāvā bija gotu kola, un nodzīvoja 256 gadus. Singāļu tautai ir sens sakāmvārds “divas lapas dienā neļaus novecot”, kas arī atspoguļo gotu kolas kā ilgmūžības auga popularitāti.

Vitamīns B9 (Folijskābe)
Vitamīns B9 jeb folijskābe ir ūdenī šķīstošs vitamīns, kas nepieciešams cilvēka imūnsistēmai, sirds, asinsvadu un asinsrades sistēmām. Cilvēka organisms nespēj sintezēt folijskābi, tāpēc tā jāuzņem ar barību. Tās lietošana pazemina homocisteīna koncentrāciju plazmā, kas savukārt potenciāli samazina kardiovaskulāro slimību risku.
B9 vitamīns, ko dēvē arī par folskābi vai folijskābi, ir viens no B grupas vitamīniem. Visi B grupas vitamīni palīdz organismam pārveidot ēdienu (ogļhidrātus) par degvielu (glikozi), kas tiek izmantota enerģijas ražošanā. Šīs grupas vitamīni palīdz organismam izmantot taukus un olbaltumvielas. B grupas vitamīni gādā par aknu veselību, skaistu ādu, matiem un veselām acīm, kā arī nodrošina normālu nervu sistēmas darbību. Folijskābe ir sintētiskā B9 vitamīna forma, kas tiek iekļauta uztura bagātinātājos un ar vitamīniem bagātinātos produktos, savukārt folskābe ir dabiski pieejama dažādos produktos.
Visi B grupas vitamīni ir ūdenī šķīstoši, proti, organismā tie neuzkrājas. Vienīgais izņēmums ir B12, kas uzkrājas aknās un tiek izmantots pēc vajadzības. Folskābe ir svarīga normālai smadzeņu darbībai, kā arī garīgās un emocionālās veselības nodrošināšanai. Tā piedalās organisma ģenētiskā materiāla — DNS un RNS — sintēzē, kas ir īpaši svarīgi straujas šūnu un audu augšanas periodā, piemēram, bērnībā, pusaudžu gados un grūtniecības laikā.
Viena no svarīgākajām reakcijām, kas nav iespējama bez folskābes, ir homocisteīna pārveidošana par metionīnu S-adenozil-metionīna sintēzes ietvaros, kas ir svarīgs metilgrupas donors. Cita no folskābes atkarīga reakcija ir deoksiuridilāta metilācija par timidilātu, veidojot DNS, kas ir obligāts šūnu dalīšanās priekšnosacījums. Šīs reakcijas traucējumi dod impulsu procesam, kas var novest pie vienas no būtiskākajām folskābes deficīta pazīmēm – megaloblastiskās anēmijas.
Folskābes deficīts parasti nav novērojams atsevišķi – to pavada citu uzturvielu deficīts, jo tas ir saistīts ar mazvērtīgu uzturu, alkoholismu un uzsūkšanās traucējumiem. Megaloblastiskā anēmija, kurai raksturīgas lieli sarkanie asinsķermenīši ar neparastu kodolu, ir primārā klīniskā pazīme, kas liecina par folskābes vai B12 vitamīna deficītu. Tai ir raksturīgi tādi simptomi kā vājums, nogurums, koncentrēšanās grūtības, aizkaitināmība, galvassāpes, sirds palpitācijas un aizdusa.
Folskābes deficīts izraisa arī mēles un mutes dobuma gļotādas jēlumus un seklas čūliņas, izmaiņas ādas, matu un rokas pirkstu pigmentācijā, gremošanas traucējumus un paaugstinātu homocisteīna līmeni asinīs.
Folskābes deficīts ir reti sastopams, taču dažiem indivīdiem tas var būt pat ekstremāli zems. Folskābes nepietiekamība var būt cilvēkiem, kas pārmērīgi lieto alkoholu, ēd mazvērtīgu pārtiku. Turklāt alkohols kavē folskābes uzsūkšanos un nonākšanu aknās, paātrina tās noārdīšanos un veicina izvadīšanu caur nierēm.
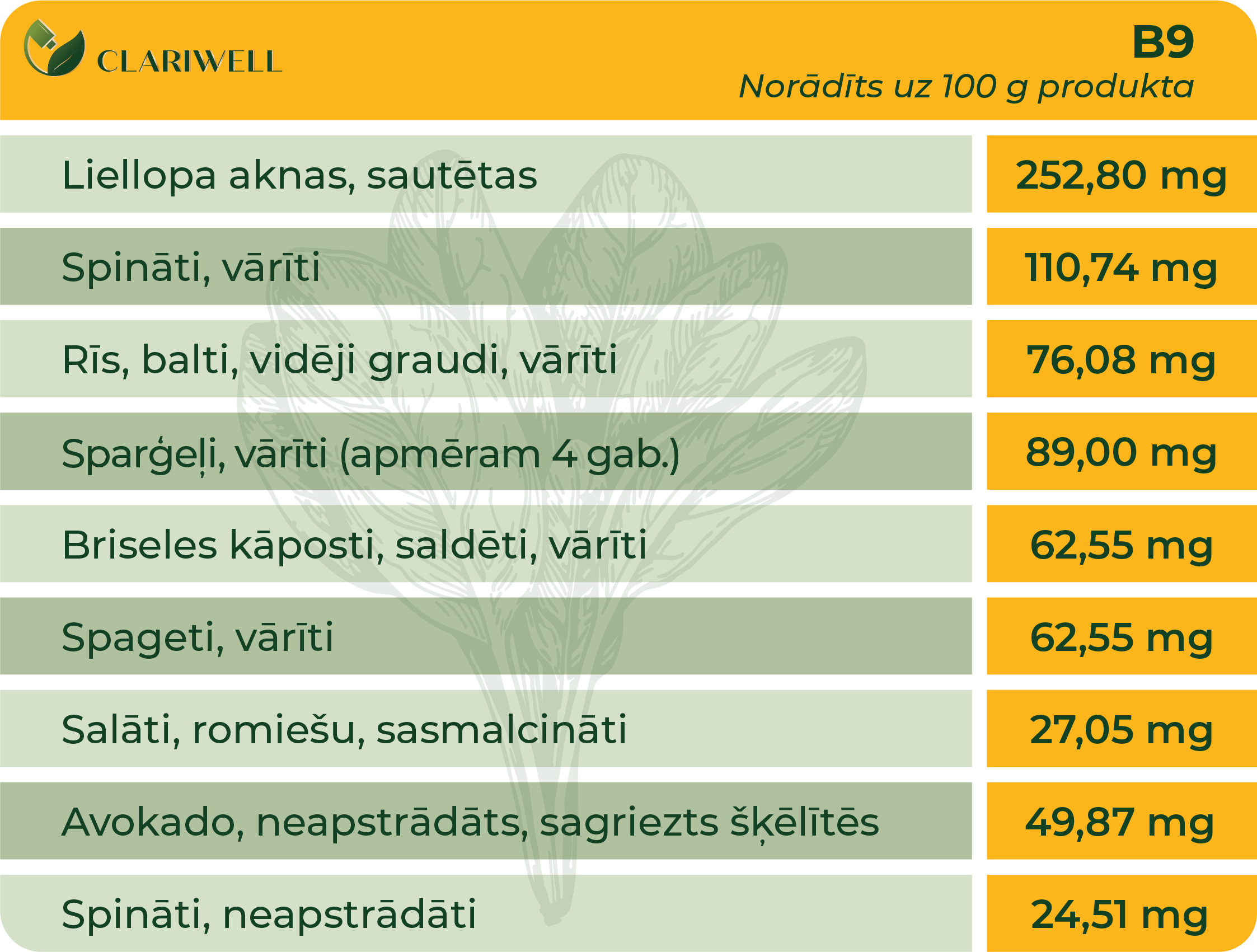
Pieaugušiem cilvēkiem, kuriem nav novērots vai apstiprināts Vitamīna B9 deficīts, normāli ir nepieciešams 400 mg (grūtniecēm 600 mg) Vitamīna B9 dienā.
Folskābes uztura bagātinātāji var ietekmēt vairāku medikamentu iedarbību. Daži piemēri ir minēti zemāk. Cilvēkiem, kas regulāri lieto šos medikamentus, vajadzētu pārrunāt iespējamo folskābes lietošanu ar savu ārstējošo ārstu.
Metotreksāts
Methotreksāts (Rheumatrex®, Trexall®), kas tiek izmantots vēža un autoimūno slimību ārstēšanā, ir folskābes antagonists. Pacientiem, kas lieto metotreksātu vēža terapijā, pirms folskābes preparātu lietošanas vajadzētu konsultēties ar onkologu, jo šis uztura bagātinātājs var ietekmēt metotreksāta pretvēža iedarbību. Taču folskābes preparāti var samazināt metotreksāta izraisītas gremošanas sistēmu skarošas blaknes, to lietojot reimatoīdā artrīta vai psoriāzes terapijā.
Pretepilepsijas medikamenti
Tādus pretepilepsijas medikamentus kā fenitoīns (Dilantin®), karbamazepīns (Carbatrol®, Equetro®, Epitol®) un valporāts (Depacon®) izmanto epilepsijas, psihisko slimību un citu veselības problēmu ārstēšanā. Šie medikamenti var samazināt folskābes līmeni serumā. Savukārt folskābes preparāti var samazināt šo medikamentu līmeni serumā, tādēļ pacientiem, kas lieto pretepilepsijas medikamentus, vajadzētu pārrunāt iespējamo folskābes preparātu lietošanu ar savu ārstējošo ārstu.
Sulfasalazīns
Sulfasalazīns (Azulfidine®) galvenokārt tiek lietots čūlainā kolīta ārstēšanai. Tas kavē folskābes uzsūkšanos zarnās un var izraisīt folskābes deficītu. Pacientiem, kas lieto sulfasalazīnu, vajadzētu pārrunāt ar savu ārstējošo ārstu nepieciešamību palielināt folskābes uzņemšanu no pārtikas, sākt lietot folskābes preparātus vai apvienot abus.
Paaugstināts homocisteīna līmenis tiek saistīts ar paaugstinātu kardiovaskulāro slimību risku. Folskābe un citi B grupas vitamīni ir iesaistīti homocisteīna vielmaiņā. Zinātnieki ir izvirzījuši hipotēzi, ka šīs mikro uzturvielas samazina kardiovaskulāro slimību risku tieši, pateicoties homocisteīna līmeņa samazināšanai.
Folijskābes (un B12 vitamīna) preparāti pazemina homocisteīna līmeni. Taču šie preparāti tiešā veidā nemazina sirds-asinsvadu slimību risku, lai gan, šķiet, rada aizsardzību pret insultu.
- Folskābi un tās lomu cilvēka bioķīmiskajos procesos atklāja pētniece Lūsija Vilsa 1931. gadā. Viņa konstatēja, ka šī uzturviela ir nepieciešama mazasinības novēršanai grūtniecības laikā.
- Folijskābe cilvēka veselībai ir ļoti svarīga, tādēļ tā tiek pievienota daudziem produktiem, it sevišķi brokastu pārslām. Procesu, kurā vitamīnus pievieno citiem produktiem, dēvē par bagātināšanu ar vitamīniem. Tādēļ, ja brokastu pārslām ir pievienoti vitamīni, tās ir ar vitamīniem bagātinātas brokastu pārslas.
- Folijskābe ir ieguvusi nosaukumu no latīņu vārda “folium”, kas nozīmē “lapa”, jo lapu dārzeņi ir bagātīgs folskābes avots.
- Folijskābes trūkums izraisa sarkano asinsķermenīšu skaita samazināšanos organismā, proti, anēmiju jeb mazasinību. Folijskābes deficīta izraisītu anēmiju dēvē par makrocitisko anēmiju. Makrocitisks nozīmē “ar lielām šūnām”. Folijskābes trūkums samazina sarkano asinsķermenīšu skaitu, un organismā cirkulējošie kļūst patiešām lieli.
- Folijskābi organisms spēj uzsūkt labāk, turklāt gandrīz divreiz labāk, nekā dabisko folskābi.

Selēns
Selēns līdzās citiem ir viens no svarīgākajiem mikroelementiem, kas nepieciešams, lai nodrošinātu cilvēka orgānu normālu darbību. Šim elementam ir svarīga loma vielmaiņā, vairogdziedzera darbībā un šūnu aizsardzībā no bojājumiem, kas saistīti ar oksidatīvo stresu. Selēns ir svarīgs arī imūnsistēmas stiprināšanai, smadzeņu darbības uzlabošanai un sirds slimību riska samazināšanai.
Selēnu 1817. gadā Zviedrijas pilsētā Gripsholmā atklāja ķīmiķis Jākobs Berzeliuss. Selēns ir dabā sastopama viela. Tas ir atrodams Zemes atmosfērā, minerālos, dzīvajā dabā un ūdenī. Šī elementa daudzums, kas konstatējams dabā un cilvēka organismā, var ļoti atšķirties atkarībā no ģeogrāfiskā reģiona un uztura.
Cilvēka organismā kopumā ir apmēram 3-20 mg selēna.
Selēns ir mikroelements, kas dabiski ir pieejams daudzos pārtikas produktos, to pievieno citiem produktiem un tas ir pieejams arī kā uztura bagātinātājs. Selēns ir dabiski nepieciešams cilvēka organismam, un tas ir vairāk nekā divdesmit selenoproteīnu sastāvā, kas ir vajadzīgi reproduktīvajai sistēmai, vairogdziedzera hormona metabolismam, DNS sintēzei un aizsardzībai pret oksidatīvo stresu un infekcijām.
Selēns ir selenoproteīnu sastāvdaļa, kam ir plaši plejotropiska (gēna izpausme vairākās pazīmēs) ietekme, sākot no antioksidanta un pretiekaisuma iedarbības līdz pat aktīva vairogdziedzera hormona sintēzei. Pēdējo 10 gadu laikā ar slimībām saistītā polimorfisma atklāšana selenoproteīnu gēnos ir ļāvusi saprast selenoproteīnu svarīgo ietekmi uz veselību. Selēna bioloģiskā nozīmība ir saistīta ar tā klātbūtni olbaltumvielu un enzīmu sastāvā. Ir konstatēti vairāki no selēna atkarīgi enzīmi, kuru aktīvajā kodolā ietilpst selēns kā selenocisteīna grupa. Vislabāk raksturojamie selenoenzīmi, kas parasti ir sastopami zīdītāju organismā, ir glutationa peroksidāze, selenoproteīns P un tiroksīna 5-deiodināze. Glutationa peroksidāze un selenoproteīns P katalizē oksidēšanās-reducēšanās reakcijas. Organisma funkcijās iesaistīti arī citi svarīgi enzīmu proteīni, piemēram, formāta dehidrogenāze, nikotīnskābes hidroksilāze, glicīna reduktāze, tiolāze un ksantīna dehidrogenāze.
Selēna deficīts tiek saistīts ar palielinātu mirstības risku, vāju imūnsistēmas darbību un kognitīvo spēju pasliktināšanos.
Ja organisms ar uzturu vai selēna uztura bagātinātājiem uzņem pietiekamu šīs minerālvielas daudzumu, tad tas spēj pretoties vīrusu ietekmei, labvēlīgi ietekmē vīriešu un sieviešu auglību, kā arī samazina autoimūno vairogdziedzera slimību risku. Daudzsološi pētījumi kopumā ir apliecinājuši, ka selēna uzņemšana pietiekamā daudzumā samazina prostatas, plaušu, kolorektālā un urīnpūšļa vēža risku, un, lai gan pētījumu secinājumi nav viennozīmīgi, ir diezgan ticams, ka uztura bagātinātāji būs iedarbīgāki, ja tiek sabalansēta arī citu uzturvielu uzņemšana.
Selēna ietekme uz veselību ir daudzšķautnaina un dažāda, tādēļ ir nepieciešams veikt papildu pētījumus, lai optimizētu šī jaudīgā mikroelementa ieguvumus un samazinātu ar to saistītos riskus.
Selēna deficīts tiek saistīts ar palielinātu mirstības risku, vāju imūnsistēmas darbību un kognitīvo spēju pasliktināšanos.
Ja organisms ar uzturu vai selēna uztura bagātinātājiem uzņem pietiekamu šīs minerālvielas daudzumu, tad tas spēj pretoties vīrusu ietekmei, labvēlīgi ietekmē vīriešu un sieviešu auglību, kā arī samazina autoimūno vairogdziedzera slimību risku. Daudzsološi pētījumi kopumā ir apliecinājuši, ka selēna uzņemšana pietiekamā daudzumā samazina prostatas, plaušu, kolorektālā un urīnpūšļa vēža risku, un, lai gan pētījumu secinājumi nav viennozīmīgi, ir diezgan ticams, ka uztura bagātinātāji būs iedarbīgāki, ja tiek sabalansēta arī citu uzturvielu uzņemšana.
Selēns uzturā:
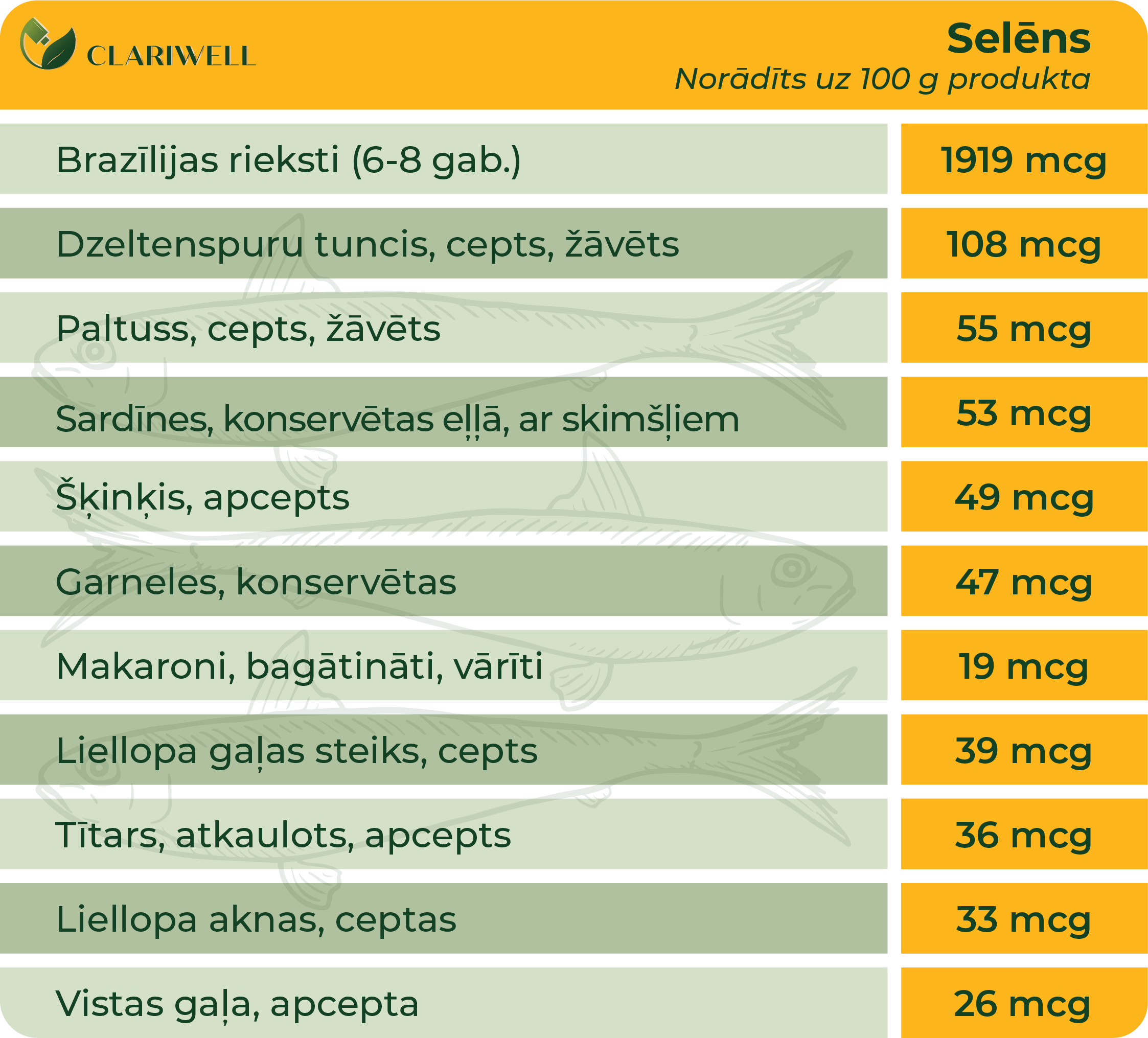
Pieaugušiem cilvēkiem, kuriem nav novērots vai apstiprināts selēna deficīts, normāli ir nepieciešams 55 mcg (mikrogrami) gan vīriešiem, gan sievietēm un 60 mcg grūtniecēm selēna dienā
Selēns var ietekmēt dažādus medikamentus, turpretim vairāki medikamenti var nelabvēlīgi ietekmēt selēna daudzumu organismā. Minēsim piemēru. Cilvēkiem, kas regulāri lieto šos un citus medikamentus, vajadzētu pārrunāt iespējamo selēna lietošanu ar savu ārstējošo ārstu.
Cisplatīns
Cisplatīns ir neorganiska uz platīna bāzes veidota ķīmijterapijas viela, ko izmanto olnīcu, urīnpūšļa, plaušu un citu vēžu ārstēšanā. Cisplatīns var samazināt selēna daudzumu matos un serumā, taču nav zināms, vai šim samazinājumam ir klīniski svarīga ietekme. Daži nelieli pētījumi ir apliecinājuši, ka selēna uztura bagātinātāju lietošana var samazināt cisplatīna toksiskumu, taču Cochrane ziņojuma autori secināja, ka nav pietiekamu pierādījumu, lai apgalvotu, ka selēna uztura bagātinātāji mazina ķīmijterapijas blaknes.
Riski veselībai no pārmērīga selēna daudzuma
Ilgstoši uzņemot lielas devas organiskā un neorganiskā selēna, var rasties līdzīga iedarbība. Agrīni simptomi, kas liecina par pārmērīgu selēna uzņemšanu ir pēc ķiplokiem smakojoša elpa un metāliska garša mutē. Visraksturīgākās ilgstoši pārmērīgi daudz uzņemta selēna pazīmes jeb selenoīze ir matu izkrišana un nagu struktūras vājināšanās jeb trauslums. Ir arī citi simptomi, piemēram, ādas un nervu sistēmas bojājumi, slikta dūša, caureja, ādas izsitumi, plankumaini zobi, nogurums, aizkaitināmība un nervus sistēmas darbības traucējumi.
Selēna deficīts
Ilgstošs selēna deficīts cilvēka organismā noved pie nopietnām slimībām. Šī elementa deficīts nelabvēlīgi ietekmē sirds-asinsvadu sistēmu un var būt miokarda infarkta cēlonis. Tas ir saistīts arī ar slimībām, kas raksturīgas konkrētam ģeogrāfiskajam reģionam: Kešana slimība un Kašina-Beka sindroms.
Epidemioloģiskie pētījumi ir ļāvuši secināt, ka vidēji smags selēna deficīts ikdienas uzturā ietekmē slimību attīstību, kuru pamatā ir novājināta imunitāte. Selēna deficīts ikdienas uzturā var nelabvēlīgi ietekmēt nervu sistēmas darbību. Cilvēkiem, kam ir selēna deficīts, ir novērojama depresijas attīstība vai trauksmes pastiprināšanās, kā arī Alcheimera slimības attīstība. Šis mikroelements tiek uzskatīts par izšķirošu HIV virulences mazināšanā un pilna spektra AIDS progresijā. Selēna deficīts grūtniecēm negatīvi ietekmē augļa attīstību. Pārmērīgs selēna daudzums var būt organismam toksisks.
Akūta saindēšanās ar selēnu ir novērojama reti. Ir grūti noteikt precīzu selēna devu, kas būtu kaitīga organismam, jo šis elements ir sastopams dažādās ķīmiskajās formās. Toksisko ietekmi uz organismu var izraisīt gan organiskās, gan neorganiskās selēna formas. Selēna toksiskums (atkarībā no devas) tiek saistīts ar konkurenci starp selēna un sēra uzsūkšanos, kas primāri ļauj sākties sēra metabolismam (transformācijai). Selēns aminoskābēs (cisteīns un metionīns) var aizstāt sēru, savukārt neorganiskie savienojumi aizstāj sēru merkapturīnskābju sintēzē un selenītu reakcijā ar tiola grupām.
Grupas, kam pastāv selēna nepietiekamības risks
Selēna deficīts ir sastopams reti un tieši tikai selēna deficīts nav bieži saistīts ar konkrētām slimībām. Tālāk minētajām grupām ir lielāka varbūtība nepietiekamā daudzumā uzņemt selēnu.
1. Cilvēki, kas mīt ar selēnu nabadzīgos reģionos
Deficīta risks pastāv cilvēkiem, kas dzīvo valstīs, kur uzturā pārsvarā lieto ar selēnu nabadzīgās augsnēs audzētus dārzeņus. Vismazāk selēnu uzņem cilvēki, kas dzīvo dažādos Ķīnas reģionos, kur iedzīvotāji pārsvarā ēd veģetāru uzturu un augsnē ir ļoti maz šī mikroelementa. Arī dažās Eiropas valstīs, it sevišķi vegānu grupā, vidējā selēna deva, kuru uzņem ikdienā ir neliela. Lai gan selēna uzņemšana Jaunzēlandē vēl nesenā pagātnē bija ļoti neliela, tā būtiski palielinājās, kad valsts uzsāka intensīvāk importēt kviešus ar augstu selēna saturu.
2. Nieru dialīzes pacienti
Salīdzinājumā ar veseliem cilvēkiem, selēna līmenis ir ievērojami zemāks pacientiem, kam ilgstoši tiek veikta hemodialīze, jo hemodialīze no asinīm izskalo selēnu. Turklāt hemodialīzes pacientiem pastāv risks uzņemt maz selēna ar pārtiku, jo urēmijas un diētas ierobežojumu dēļ viņiem mēdz būt anoreksija. Lai gan selēna uzņemšana uztura bagātinātāju veidā hemodialīzes pacientiem palielina šī mikroelementa daudzumu asinīs, ir nepieciešami vairāk pierādījumu, lai noteiktu, vai uztura bagātinātājiem ir labvēlīga klīniskā ietekme uz šo cilvēku grupu.
3. HIV pacienti
Parasti HIV pacientiem ir zems selēna līmenis, jo, iespējams, viņi par maz to uzņem ar uzturu (it sevišķi jaunattīstības valstīs), rodas pārmērīgs zudums caurejas un uzsūkšanās traucējumu dēļ. Novērojuma pētījumi ir ļāvuši konstatēt saikni starp zemu selēna koncentrāciju HIV pacientu asinīs un palielinātu kardiomiopātijas, nāves risku un grūtniecēm – HIV transmisiju bērnam un bērna agrīnu nāvi.
Daži fakti norāda uz selēna lomu smadzeņu funkcijās: samazinoties selēna līmenim organismā, smadzenes atlikušo saņems primāri; pie selēna deficīta mainās vairāku neirotrnsmiteru cirkulācijas ātrums; selēnu saturošu uztura bagātinātāju lietošana samazina neatrisināmas epilepsijas lēkmes bērniem; maza selēna koncentrācija plazmā gados vecākiem cilvēkiem būtiski korelē ar senilitāti un ātrāku kognitīvo spēju mazināšanos, savukārt Alcheimera pacientiem, salīdzinājumā ar kontroles grupu, selēna koncentrācija smadzenēs bija tikai 60%.
Turklāt smadzenēm trūkst katalāzes, tādēļ peroksidācijas produkti, piemēram, ūdeņraža peroksīds un primārie peroksīdi, ir jāizvada ar antioksidantu – selenoenzīmu – palīdzību.
Pietiekama selēna daudzuma labvēlīgā ietekme uz noskaņojumu ir novērojama vismaz tad, kad selēna daudzums ir “uz nepietiekamības sliekšņa”. Trijos pētījumos selēna deficīts bija saistīts ar būtiski lielāku depresijas iespējamību un citu negatīvu ietekmi uz noskaņojumu, piemēram, trauksmi, apmulsumu un naidīgumu.
Selēna koncentrācija serumā ar gadiem mazinās. Margināls selēna koncentrācijas deficīts var būt saistīts ar smadzeņu funkcijas pavājināšanos vecuma ietekmē, kam ir iespējama saistība ar selēna antioksidanta iedarbību.
Selēns, kas atrodas konkrētu selenoenzīmu sastāvā, ir būtisks pareizai vairogdziedzera darbībai un tas pasargā šūnas no oksidatīvā bojājuma, ko izraisa H2O2 vairogdziedzera hormonu sintēze, un viens pētījums ir parādījis, ka oksidatīvā stresa marķieri ir saistīti ar kognitīvo spēju pasliktināšanos iedzīvotāju grupā, kurā parasti ir spēcīgi kognitīvie rādītāji.
No selēna atkarīgā glutationa reduktāze un selenoproteīni ir būtiski antioksidantu mehānismam, kas ir neaizstājams organisma aizsargs. Selēns ietekmē vielmaiņas ceļus, mainot selenoproteīnu aktivitāti, un tas spēlē zināmu lomu šūnu aizsardzībā pret oksidatīvo stresu. Selēna koncentrācija regulē selenoproteīnu ekspresiju. Mainīga selēna koncentrācija var dažādi ietekmēt imunitāti un enerģijas vielmaiņu. Jaunākajos pētījumos paaugstināti stresa biomarķieri ir novēroti depresijas gadījumā, un tas norāda uz to, ka oksidatīvais stress var būt svarīgs depresijas rašanās un attīstības faktors. Selēns var būt aizsargājošs faktors, kas mazina trauksmi un depresiju, iespējams, pateicoties tā aizsargājošajai ietekmei pret oksidatīvo stresu.
Un visbeidzot jāpiemin, ka selēnam var būt antidepresanta iedarbība, jo tas ietekmē dažādas neirotransmiteru sistēmas. Ir secināts, ka selēnam ir modulējoša ietekme uz dopamīnerģisko, serotonīnerģisko un noradrenerģisko sistēmu, kas visas ir iesaistītas depresijas un citu garīgo slimību patofizioloģijā.
- Selēns ilgstoši tika uzskatīts par indīgu vielu. Saindēšanās ar to noveda pie smagas anēmijas, kaulu stīvuma, matu izkrišanas un akluma. Šie simptomi bija novērojami cilvēkiem un dzīvniekiem, kas dzīvoja reģionos, kur šī mikroelementa saturs augsnē bija apmēram 1000 reizes lielāks, salīdzinājumā ar augsni citos pasaules reģionos ar vidēju selēna koncentrāciju.
- Selēna nosaukums ir atvasināts no grieķu vārda “selene”, kas nozīmē “mēness”. Senajā Grieķijā Selēna bija Mēness dieviete.
- Selēns ir nemetāls. Līdzīgi kā citiem nemetāliem, arī selēnam ir atšķirīgas krāsas un struktūras (allotropi), ko ietekmē konkrēti stāvokļi.
- Brazīlijas rieksti satur daudz selēna, arī tad, ja tie audzēti augsnē, kura nav bagāta ar šo mikroelementu. Viens rieksts satur selēna dienas devu pieaugušajam.
- Selēnu sākotnēji izmantoja, lai noņemtu stiklam pigmentu, lai iekrāsotu stiklu sarkanu un lai iegūtu pigmentu “Ķīnas sarkanais”. To izmanto arī lāzerprinteru un fotokopētāju fotoelementā, tēraudā, pusvadītājos un dažos medicīnas preparātos.
- Selēns pasargā no saindēšanās ar dzīvsudrabu.
Cilvēkiem būtiskais mikroelements selēns tiešā veidā iedarbojas uz vairogdziedzera hormonu metabolismu (vielmaiņu) un oksidēšanās – reducēšanās procesiem. Vairogdziedzera darbība ir kritiski atkarīga no joda un selēna, lai nodrošinātu tā pilnvērtīgu darbību. Nepietiekošs selēna daudzums organismā ir saistīts ar paaugstinātu vairogdziedzera slimību risku.1
Selēnu var uzskatīt par vairogdziedzera veselības atslēgu. Tas ir nepieciešams mikroelements vairogdziedzera hormonu sintēzei un darbībai. Selēna koncentrācija vairogdziedzerī ir augstāka nekā jebkurā citā ķermeņa orgānā. Selēns darbojas kopā ar jodu, lai aktivizētu trīs dažādas no selēna atkarīgās jodotironīna dejodināzes, kas pēc tam var aktivizēt vai deaktivizēt vairogdziedzera hormonus.Visas trīs dejodināžu izoformas ir selēnu saturoši enzīmi, tāpēc ar uzturu vai uztura bagātinātājiem iegūtais selēns ir būtisks trijodtironīna (T3) ražošanai. Šis process (un selēns) ir būtisks normālai augšanai, attīstībai un vielmaiņai.2
Selēna deficīts ir saistīts ar hipotireozi, Hašimoto slimību, palielinātu vairogdziedzeri, vairogdziedzera vēzi un Greivsa slimību.
Viens pētījums ar 1900 dalībniekiem atklāja sakarību starp selēna koncentrāciju serumā un vairogdziedzera izmēru. Tika novērotaselēna aizsargājošā iedarbība pret palielinātu vairogdziedzeri un vairogdziedzera audu bojājumiem. Šajā konkrētajā pētījumā šie rezultāti bija nozīmīgi tikai dalībniecēm sievietēm3.
Citā pētījumā tika aplūkota selēna ietekme uz Greivsa orbitopātiju(kad vairogdziedzeris ražo pārāk daudz vairogdziedzera hormona). Pētnieki salīdzināja ārstēšanu ar selēnu ar ārstēšanu ar pentoksifilīnu(Pentilin), kas ir pretiekaisuma līdzeklis. Selēna terapijas grupa ziņoja par uzlabotu dzīves kvalitāti un palēninātu Greivsa orbitopātijas progresēšanu salīdzinājumā ar pentoksifilīna (Pentilin)terapijas grupu.4

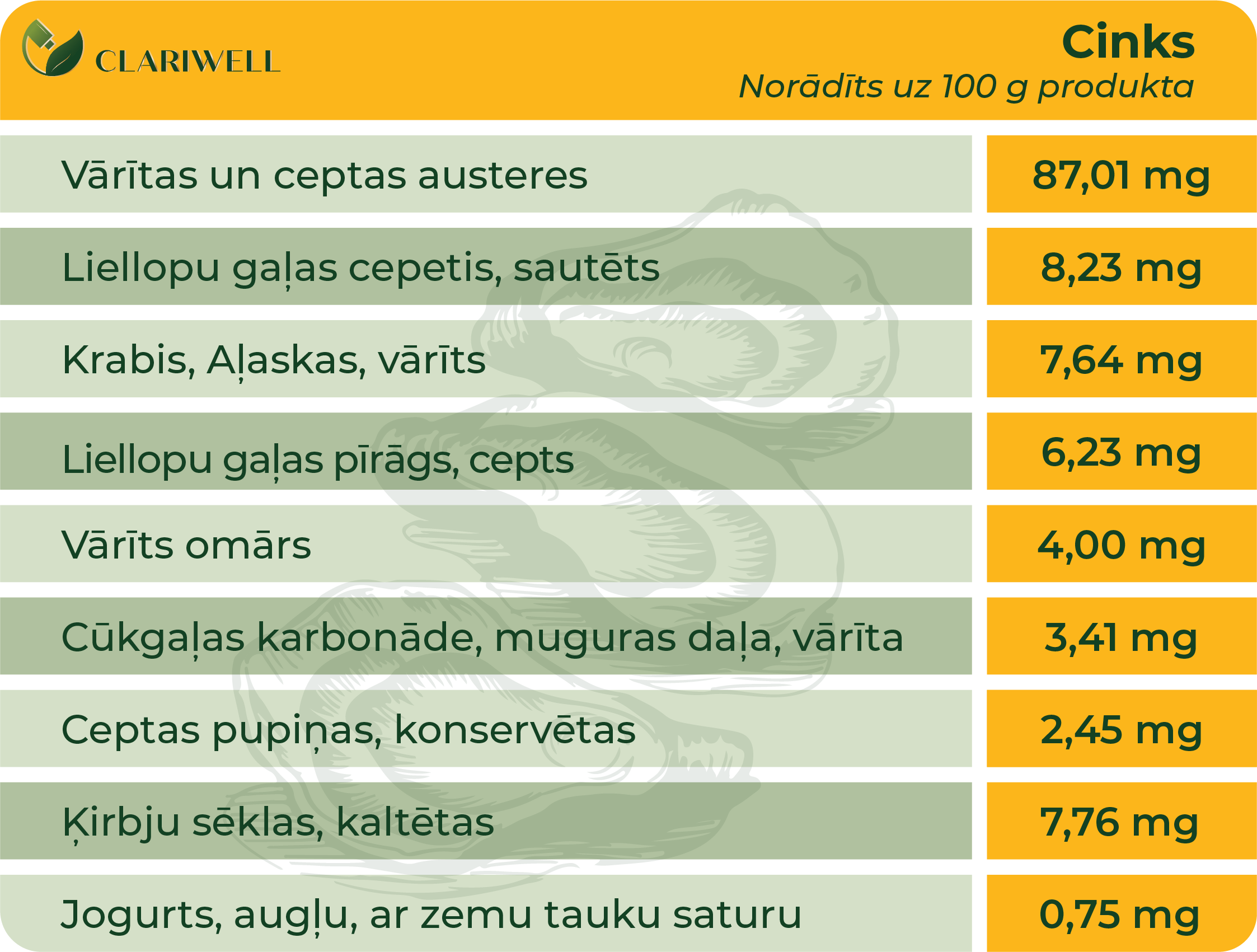
Cinks
Cinks ir viens no svarīgākajiem mikroelementiem cilvēka organismā. Tas ir nepieciešams olbaltumvielu sintēzei, kā arī svarīgu hormonu ražošanai. Hronisks cinka deficīts var izraisīt neiroloģiskus un garīgus traucējumus, piemēram, depresiju. Cinkam ir izšķiroša nozīme pareizai vairogdziedzera hormonu vielmaiņai; cinka deficīts var izraisīt vairogdziedzera hormonu līmeņa pazemināšanos un vielmaiņas ātrumu miera stāvoklī. Cinks spēcina imūno sistēmu. Tam ir sava loma visos imūnās funkcijas aspektos, tajā skaitā izšķirīga nozīme T-šūnu (galveno imūnšūnu) attīstībā un aizkrūtes dziedzera (galvenais imunitātes ģenēzes orgāns) atjaunošanā.
Cinks ir svarīgs bioloģiskais elements, kam ir būtiska loma plaša spektra bioķīmiskajos procesos. Šis metāls ir viena no galvenajām dažādu olbaltumvielu sastāvdaļām un svarīgs imūnsistēmas un nervu sistēmas modulators. Tas ir otrs visbiežāk sastopamais metāliskais mikroelements cilvēka organismā pēc dzelzs un vienīgais metāls, kas ir klātesošs visās enzīmu klasēs.
Cinks ir iesaistīts daudzos šūnu vielmaiņu aspektos. Tas ir nepieciešams vairāk nekā 300 enzīmu un 1000 transkripcijas faktoru katalītiskajai aktivitātei un spēlē būtisku lomu imunitātes funkcijā, olbaltumvielu sintēzē, brūču dzīšanā, DNS sintēzē un šūnu dalīšanās procesā. Cinks arī veicina normālu augšanu un attīstību grūtniecības laikā, bērnībā un pusaudžu gados, un tas ir nepieciešams izteiktai garšas un ožas sajūtai.
Smadzenēs glutamāterģiskie neironi noglabā cinku īpašos sinapšu pūslīšos, un tas var modulēt neironu ierosu. Tas pilda galveno lomu sinapšu plasticitātē un arī spējā mācīties. Cinka homeostāzei arī ir izšķiroša loma funkcionālā centrālās nervu sistēmas regulēšanā. Cinka homeostāzes regulācijas traucējumi centrālajā nervu sistēmā noved pie pārmērīgas cinka koncentrācijas sinapsēs, un tas, šķiet, izraisa neirotoksicitāti caur mitohondriju oksidatīvā stresa mehānismu (piem., neļaujot darboties konkrētiem enzīmiem, kas ir iesaistīti elektronu transportēšanas ķēdē), kalcija homeostāzes regulācijas traucējumus, glutamāterģisko neironu eksotoksicitāti un starpneironu signālu vadīšanas traucējumus.
Vienlaikus pētījumi ir pierādījuši korelāciju starp cinka deficītu un vairogdziedzera hormonu līmeni. Cinks ir nepieciešams pareizai enzīma dejodināzes darbībai, kas aktivizē neaktīvo tiroksīna (T4) hormonu par aktīvāku formu - trijodtironīnu (T3), nodrošinot visas vairogdziedzera funkcijas cilvēka organismā.
Cinks ietekmē vairākus imūnsistēmas aspektus. Tam ir izšķiroša nozīme iedzimto imunitātes šūnu, neitrofilu un galētājšūnu (naturālie killeri jeb NK šūnas) normālā attīstībā un darbības nodrošināšanā. Cinka deficīts ietekmē arī makrofāgus – lielas šūnas, kas ievelk un sagremo organismam svešas daļiņas. Cinka deficīts ietekmē fagocitozi, intracelulāro nogalināšanu un citokīnu veidošanos. Cinka deficīts negatīvi ietekmē T un B šūnu augšanu un darbību. Cinka spēja darboties kā antioksidantam un stabilizēt membrānas liecina, ka tam ir nozīme brīvo radikāļu izraisītu traumu novēršanā iekaisuma procesu laikā.
Cinka deficīts
Cinka deficītam ir raksturīgi augšanas traucējumi, apetītes zudums un pavājināta imūnsistēmas darbība. Smagākos gadījumos cinka deficīts izraisa matu izkrišanu, caureju, vēlīnu dzimumbriedumu, impotenci, samazinātus vīriešu dzimumorgānus, acu un ādas bojājumus. Tas var izraisīt arī svara zudumu, pasliktināt brūču dzīšanu, radīt garšas sajūtas traucējumus un prāta letarģiju. Daudzi no šiem simptomiem nav specifiski un bieži vien ir saistīti arī ar citām veselības problēmām, tādēļ, lai pārliecinātos par cinka deficītu, ir nepieciešams veikt medicīnisku pārbaudi. Cilvēkiem, kam ir cinka deficīta vai nepietiekamības risks, savā ikdienas uzturā vajadzētu iekļaut pietiekami daudz cinku saturošu produktu.
Grupas, kam pastāv cinka nepietiekamības risks
1. Cilvēki ar kuņģa-zarnu trakta un citām slimībām
Cilvēkiem, kam ir veikta kuņģa-zarnu trakta operācija un ir gremošanas problēmas (piemēram, čūlainais kolīts, Krona slimība un īsās zarnas sindroms), var pasliktināties cinka uzsūkšanās spēja un palielināties iekšēja cinka zudumi, galvenokārt no kuņģa-zarnu trakta un mazāk no nierēm. Citas ar cinka deficītu saistītas slimības ir malabsorbcijas (vājas uzsūkšanās) sindroms, hroniskā aknu slimība, hroniskā nieru slimība, sirpjveida šūnu anēmija, diabēts, onkoloģiskās slimības un citas hroniskās kaites. Arī hroniska caureja paātrina cinka izvadīšanu no organisma.
2. Veģetārieši
Cinka biopieejamība no veģetāra uztura ir mazāka nekā no visēdāja ēdienkartes, jo veģetārieši neēd gaļu, kas satur daudz biopieejamā cinka, kas var veicināt tā uzsūkšanos. Turklāt veģetārieši parasti ēd vairāk pākšaugus un pilngraudu produktus, kas satur fitātus, kuri piesaistās cinkam un kavē tā uzsūkšanos.
3. Grūtnieces un ar krūti barojošas māmiņas
Grūtniecēm, it sevišķi tām, kurām grūtniecības sākumā ir ļoti zems cinka līmenis, ir īpaši liels risks iemantot cinka deficītu, galvenokārt tādēļ, ka auglim ir nepieciešams daudz cinka. Arī barošana ar krūti var noplicināt māmiņas cinka krājumus.
4. Lielāki bērni, kurus joprojām baro tikai ar krūti
Mātes piens nodrošina pietiekamu cinka daudzumu (2 mg/dienā) pirmos 4-6 dzīves mēnešus, taču nenodrošina ieteicamo cinka devu mazuļiem no 7 līdz 12 mēnešu vecumam, kuriem šī prasība ir 3 mg/dienā. Bērniem, kas sasnieguši 7-12 mēnešu vecumu, papildus mātes pienam vajadzētu ēst savam vecumam piemērotu pārtiku vai piena maisījumu, kura sastāvā ir iekļauts cinks. Cinka uztura bagātinātāju lietošana dažiem bērniem, kam ir novērojami viegli līdz vidēji augšanas traucējumi un cinka deficīts, ir uzlabojusi augšanas ātrumu.
5. Cilvēki ar sipjveida šūnu anēmiju
Liela šķērsgriezuma apsekojuma rezultāti liecina, ka 44% bērnu, kam ir sirpjveida šūnu anēmija, ir zema cinka koncentrācija plazmā, iespējams, lielākas nepieciešamības pēc šīs uzturvielas un/vai nabadzīgāka uztura dēļ. Cinka deficīts ietekmē arī aptuveni 60%-70% pieaugušo ar sirpjveida šūnu anēmiju.
6. Alkoholiķi
Apmēram 30-50% alkoholiķu ir zems cinka līmenis, jo etanola patēriņš samazina cinka uzsūkšanos zarnās un palielina tā izvadīšanu ar urīnu. Turklāt daudzu alkoholiķu ēdienkarte un apēstais pārtikas daudzums ir ierobežots, novedot pie nepietiekamas cinka uzņemšanas. 6
Cinks uzturā. Pieaugušiem cilvēkiem, kuriem nav novērots vai apstiprināts Cinka deficīts, normāli ir nepieciešams 11 mg vīriešiem, 8 mg sievietēm un 11 mg grūtniecēm Cinka dienā
Cinku saturoši uztura bagātinātāji var miiedarboties ar vairākiem medikamentu veidiem. Daži piemērus šeit minēsim. Cilvēkiem, kas regulāri lieto šos medikamentus, vajadzētu pārrunāt iespējamo cinka lietošanu ar savu ārstējošo ārstu.
1.Antibiotikas
Gan kvinolona antibiotikas (piemēram, Cipro®), gan tetraciklīna antibiotikas (piemēram, Achromycin® un Sumycin®) mijiedarbojas ar cinku gremošanas traktā, kavējot gan cinka, gan antibiotiku uzsūkšanos. Šo mijiedarbību var samazināt, lietojot antibiotikas vismaz 2 stundas pirms vai 4-6 stundas pēc cinka uztura bagātinātāju lietošanas.
2.Penicilamīns
Cinks var samazināt reimatoīdā artrīta ārstēšanā izmantotā penicilamīna uzsūkšanos un iedarbību. Lai samazinātu šo mijiedarbību, pacientiem vajadzētu lietot cinka uztura bagātinātājus vismaz 2 stundas pirms vai pēc penicilamīna lietošanas.
3.Diurētiķi
Tiazīda diurētiķi, piemēram, hlortialidona (Hygroton®) un hidrohlorotiazīda (Esidrix® and HydroDIURIL®) lietošana par 60% pastiprina cinka izvadīšanu no organisma ar urīnu. Ilgstoša tiazīda diurētiķu lietošana var samazināt cinka krājumus audos, tādēļ, ja tiek lietoti šie medikamenti, ārstiem būtu jāuzrauga pacientu cinka līmenis.
Cilvēka smadzenēs ir atrodama liela cinka koncentrācija. Depresijas pacienti, iespējams, ēd pārāk maz cinku saturošus produktu un pastāvīga cinka nepietiekamība pārtikā var veicināt depresijas simptomus, vēl vairāk samazinot funkcijām pieejamo cinku, tādēļ cinku saturoši uztura bagātināji var ietekmēt depresijas simptomus. Pirmsklīniskajos pētījumos ārstēšana tikai ar cinku vai ilgstoša ārstēšana ar cinku ir apliecinājusi antidepresantiem līdzīgu ietekmi.
Saskaņā ar nesen izteiktu hipotēzi par antidepresantu iedarbību, viens no galvenajiem mērķiem, ko antidepresantam vajadzētu mainīt, ir NMDA glutamāta receptors. Cinka antidepresanta iedarbības mehānisms varētu būt saistīts ar to, ka tas ir tiešais NMDA receptora antagonists. Cinks ir iesaistīts ne tikai CNS darbībā, bet arī imunitātes/iekaisuma regulācijā, kas ir raksturīga depresīviem traucējumiem.
Hipokampā un smadzeņu garozā cinka joni regulē sinapses transmisiju vai darbojas kā neirotransmiteri, modulējot daudzus ligandu un sprieguma kontrolētus jonu kanālus. Cinka homeostāzes traucējumi šajos apgabalos ir netieši saistīti ar daudziem kognitīvajiem, uzvedības un emocionālās regulācijas traucējumiem caur samazinātas neiroģenēzes un neiroplasticitātes mehānismiem.
Cinka deficīts ir arī netieši iesaistīs endokrīnajā depresijas ķēdē. Pastāvīgi augsts kortizola līmenis ir saistīs ar depresijas attīstību caur hipotalāma-hipofīzes-virsnieru (HHV) ass hiperaktivitāti. Līdz ar to paaugstināts kortizola līmenis plazmā var ietekmēt saikni starp cinka deficītu un depresiju.
Attiecības starp cinka līmeni serumā un depresiju var daļēji skaidrot ar atgriezenisko cēloņsakarību, jo depresija ietekmē cinka uzņemšanu, biopieejamību vai bioloģisko regulāciju. Oksidatīvais stress un to pavadošā imūnā iekaisuma reakcija var būt saistīta ar depresijas patofizioloģiju. Oksidatīvais stress palielina iekaisumu izraisošo citokīnu (piem., interleikīna 1 (IL-1) un IL-6) daudzumu, vienlaikus samazinot albumīna daudzumu un palielinot metalotioneīnu sintēzi. Albumīns ir galvenais cinka transportētājs, un albumīna daudzuma samazināšanās paralēli metalotioneīnu daudzuma kāpumam var kopīgi samazināt cinka daudzumu serumā.
Cinks ir būtisks elements, kas iesaistīts daudzās vairogdziedzera pamata bioķīmiskās reakcijās. Cinks ir nepieciešams hormonu trijodtironīna (T3), tiroksīna (T4) un vairogdziedzeri stimulējošā hormona (TSH) ražošanai.
T4 ir vairogdziedzera pamathormons, kas ir savdabīga organisma rezerve, savukārt T3 ir daudz aktīvāks hormons. Vajadzības gadījumā no T4 atdalās viena joda molekula, un tas pārvēršas aktīvā hormonā - T3.
Šis mikroelements piedalās tirotropīnu atbrīvojošā hormona (TRH) sintēzē hipotalāmā un tirotropīna vai vairogdziedzera stimulējošā hormona (TSH) sintēzē hipofīzē.1
Daži pētījumi ir uzrādījuši, ka cinka deficīts un zema cinka koncentrācija asins serumā var izraisīt izmaiņas vairogdziedzera struktūrā un vairogdziedzera hormonu vielmaiņā. Tāpat pētījumi ir pierādījuši, ka, lietojot cinku, var palielināt vairogdziedzera hormonu koncentrāciju.1
Pētījumā, kur personas papildus lietoja cinku, tām uzlabojās visi vairogdziedzera hormonu līmeņi (īpaši T3), kā arī vielmaiņas ātrums miera stāvoklī. Cits pētījums pierādīja, ka cinka lietošana atsevišķi vai kombinācijā ar selēnu var uzlabot vairogdziedzera darbību sievietēm ar hipotireozi.2
Cinka trūkums var izraisīt hipotireozi. No otras puses, hipotireoze var izraisīt cinka deficītu, jo vairogdziedzera hormoni ir nepieciešami cinka uzsūkšanai.
Ir konstatēts, ka cinks ir būtisks mikroelements imūnsistēmai. Tomēr šūnu un molekulārā līmenī, cinka iedarbības mehānismi uz imūnsistēmu ir noskaidroti salīdzinoši nesen un tā iedarbība ir daudzpusīga.
Atbilstošs cinka līmenis organismā ir būtisks, lai nodrošinātu dažādu limfocītu (galvenās imūnšūnas) populāciju veidošanos un darbību, piemēram, T-šūnu (jeb T limfocītu) dalīšanos, nobriešanu un diferenciāciju (attīstīšanos dažādās formās); limfocītu atbildes reakciju uz mitogēniem (mazi bioaktīvi proteīni vai peptīdi, kas rosina šūnu sākt šūnu dalīšanos vai palielina dalīšanās ātrumu). Vienlaikus cinks ir svarīgs, lai ieprogrammētu limfoidās un mieloīdas izcelsmes šūnu nāvi; gēnu transkripciju un biomembrānas funkciju. Limfocīti ir viens no šūnu veidiem, ko aktivizē tieši cinks. Cinks ir dažādu proteīnu, neiropeptīdu, hormonu receptoru un polinukleotīdu strukturālā sastāvdaļa. Cinka deficīts izraisa ātru un izteiktu aizkrūtes dziedzera atrofiju, šūnu izraisītus ādas jutības traucējumus un limfopēniju. Cinka deficīta gadījumā samazinās primārās un sekundārās antivielu atbildes reakcijas, īpaši tiem antigēniem, kuriem nepieciešama T-šūnu palīdzība, piemēram, tiem, kas atrodas heterologajās sarkanajās asins šūnās. Turklāt samazinās antivielu reakcija un liesā esošo citotoksisko T šūnu veidošanās pēc imunizācijas. Cinks arī inhibē audzēja nekrozes faktora veidošanos, kas ir saistīts ar kaheksijas patofizioloģiju un iegūtā imūndeficīta sindromu.
Vienkāršāk sakot, cinks ir absolūti svarīgs aizkrūtes dziedzera funkcionēšanai un imūnās sistēmas normālai darbībai. Cinks novērš imūndeficīta rašanos, stimulējot antivielu sintēzi un nodrošinot pretvīrusu iedarbību.
- Šis elements iespējams tika nosaukts par godu alķīmiķim Paracelzam, atvasinot no vācu vārda “Zinke”, kas apzīmē “zobam līdzīgais, asais vai robainais” (metāliskiem cinka kristāliem ir adataina forma). Cinks var netieši nozīmēt arī “alvai līdzīgais”, jo tam ir saikne ar vācu valodas vārdu “zinn”, kas apzīmē alvu.
- Senākās zināmās tabletes tika izgatavotas no cinka karbonāta – hidrocinkīta un smitsonīta. Šīs tabletes lietoja iekaisušu acu ārstēšanai, un tās tika atrastas uz romiešu kuģa Relitto del Pozzino klāja, kas aizgāja bojā 140. g. pr. Kr.
- Alķīmiķi dedzināja cinka metālu gaisā un ievāca kondensatorā izgarojušo cinka oksīdu. Daži alķīmiķi šo cinka oksīdu dēvēja par “lana philosophica”, kas latīņu valodā nozīmē “filozofu vilna”, jo tas veidoja vilnai līdzīgus kušķus, turpretī citi uzskatīja, ka tas izskatās pēc balta sniega un nodēvēja to par “nix album”.
- Cinks ir dabisks kukaiņu atbaidītājs un saules aizsargkrēms, kas pasargā lūpas un ādu.
- Cinks ir 100% pārstrādājams. Šobrīd vairāk nekā 80% pasaulē pieejamā cinka tiek pārstrādāts.

GABA (gamma-aminosviestskābe)
Gamma-aminosviestskābe (GABA) ir viena no vissvarīgākajām asins un smadzeņu sastāvdaļām, tā spēj uzlabot smadzeņu asins apgādi, aktivizēt enerģijas procesus un palielināt audu elpošanas aktivitāti. Turklāt tā paātrina glikozes izmantošanu un palīdz izvadīt toksiskos vielmaiņas produktus. GABA lietošana palīdz novērst nelīdzsvarotību, kas saistīta ar trauksmi, tai ir relaksējoša un nomierinoša iedarbība.
Gamma-aminosviestskābe (GABA) tika atklāta 1950. gadā, un tā ir aminoskābe, ko dabiski ražo smadzenes. GABA darbojas kā neirotransmiteris, nodrošinot smadzeņu šūnu saziņu. GABA galvenā loma mūsu organismā ir smadzeņu un centrālās nervu sistēmas (CNS) neironu aktivitātes samazināšana, kas savukārt daudzveidīgi ietekmē gan ķermeni, gan prātu, tostarp veicina atslābināšanos, samazina stresu, rada mieru, līdzsvaro noskaņojumu, atvieglo sāpes un uzlabo miegu.
Aminoskābju neirotransmiteri ir ļoti svarīgi CNS darbībai; tie darbojas ātri, izsaucot reakciju dažu milisekunžu laikā, tādēļ šai vielai ir svarīga loma smadzeņu funkcijās un neiroloģisko slimību gadījumā.
Stresa apstākļos tiek patērēti konkrēti metabolīti (vielmaiņu produkti), piemēram GABA, un to aizstāšanai ir nepieciešamas papildu uzturvielas. Tā kā uzturvielu daudzums dažādiem cilvēkiem var būt atšķirīgs, un šīs uzturvielas ir grūti iegūt no pārtikas, labāka alternatīva ir lietot nepieciešamās papildu uzturvielas kā bagātinātu funkcionālo pārtiku un/vai uztura bagātinātājus.
GABA audos tiek sintezēts no glutamīnskābes ar enzīma glutamīnskābes dekarboksilāzes (GAD) palīdzību ar piridoksal-5-fosfātu (P5P) kā kofaktoru.
Ārpus CNS, GABA sintezē resnajā zarnā mītošā mikroflora. GABA kā galvenais kavējošais neirotransmiteris pretdarbojas pārmērīgam smadzeņu uzbudinājumam, un to var aprakstīt kā neironu kontūra “bremzes” paaugstināta stresa apstākļos. Kad GABA ir atbrīvota no GABA-erģiskajiem nervgaliem, tā iedarbojas kavējoši gan uz GABA-A, gan GABA-B receptoriem.
GABA-A receptori regulē smadzeņu ierosu un atbild par tūlītēju GABA izraisītu kavējošu iedarbību uz sinapsēm. Tā kā zems GABA līmenis tiek saistīts ar trauksmi, depresiju, bezmiegu un epilepsiju, ir izveidoti medikamenti, kas ir vērsti uz šiem GABA receptoriem. Ankiolītisku, sāpju noņemošu, pretkonvulsiju un nomierinošu iedarbību, modulējot GABA-A receptoru aktivitāti vai bloķējot GABA atkaluzņemšanu caur GABA transportētāju (GAT) olbaltumvielām, rada vairāki medikamenti, alkohols un psihoaktīvas zāles.
Papildus ietekmei uz smadzenēm, ir pierādīts, ka lielas GABA devas (5-10 g vienā devā) ietekmē endokrīno sistēmu, tostarp palielina augšanas hormona līmeni plazmā, lai gan šīs ietekmes klīniskais nozīmīgums šobrīd nav zināms.
GABA (gamma-aminosviestskābe) deficīts
Cilvēkiem ar dažām veselības problēmām var būt zemāks GABA līmenis. Dažas no tām:
- Slimības, kas izraisa krampjus
- Trauksme
- Hronisks stress
- Depresija
- Grūtības koncentrēties un atmiņas problēmas
- Muskuļu sāpes un galvassāpes
- Bezmiegs un citas miega problēmas
- Vāja GABA aktivitāte ir saistīta arī ar apreibinošu vielu lietošanu.
Daži cilvēki, kam ir minētās problēmas, lieto GABA uztura bagātinātājus, lai labāk kontrolētu simptomus, taču GABA dabiski ir atrodams arī zaļajā, melnajā un oolong tējā, kā arī fermentētos produktos, piemēram, kefīrā, jogurtā un tempē. Citi produkti, kas satur GABA vai var uzlabot tā veidošanos organismā, ir pilngraudi, baltās pupas, soja, lēcas un citas pupiņas, rieksti, tostarp valrieksti, mandeles un saulespuķu sēklas, zivis, tostarp garneles un butes, citrusaugļi, tomāti, ogas, spināti, brokoļi, kartupeļi un kakao. Taču šiem simptomiem var būt psiholoģiski un fiziski cēloņi, tādēļ labāk pārrunājiet ar savu ārstu pirms ķeraties pie ārstēšanas ar uztura bagātinātājiem.
GABA lietošana tādās devās, kāda ir atrodama pārtikā, visticamāk, ir droša. Iespējams, ka to ir droši lietot lielākās devās kā medikamentu. Ir dati par devām līdz 1,5 gramiem dienā līdz viena mēneša kursam.
1) Nav ieteicams lietot grūtniecības un laktācijas laikā.
2) GABA var samazināt asinsspiedienu tiem, kam tas parasti ir augsts. Ja jūs lietojat GABA papildus asinsspiedienu regulējošajiem medikamentiem, jūsu asinsspiediens var nokristies pārāk zemu.
3) Pacientiem, kas lieto sintētiskos GABA antagonistu medikamentus vai garšaugus, kas mijiedarbojas ar GABAerģisko sistēmu (piem., balderiāņus, divšķautņu asinszāli), jābūt piesardzīgiem lietošanā.
Ja ir nepieciešams papildu nomierinošs/atslābinošs efekts, sāciet lietot GABA saturošus uztura bagātinātājus pakāpeniski un nelielās devās.
GABA antagonistu medikamenti: Baclofen, Zolpidem, Progabide, AZD 3355, Tramiprosate, Gaboxadol, Adipiplon, Arbaclofen Placarbil, Lesogaberan, Muscimol, Phenibut, Zaleplon u. c.
4) Pretēji sintētiskajiem GABA antagonistu medikamentiem, dabiskais GABA gandrīz nerada nekādas blaknes.
Iespējamās blaknes
Veseli cilvēki kopumā labi panes GABA orāli lietojamos uztura bagātinātājus. Dažiem var būt nepatīkamas blaknes, tostarp:
- Gremošanas traucējumi.
- Slikta dūša.
- Samazināta apetīte.
- Aizcietējumi.
- Dedzinoša sajūta kaklā.
- Miegainība un nogurums.
- Muskuļu vājums.
- Elpas trūkums, lietojot ļoti lielas devas
Vispārēji depresīvie traucējumi (VDT) ietekmē vairāk nekā 300 miljonus cilvēku, un saistībā ar VDT ārstēšanas pieejamības un efektivitātes ierobežojumiem, tā ir kļuvusi par vadošo invaliditātes cēloni pasaulē. Neskatoties uz ilgstošiem centieniem identificēt depresijas izcelsmes un attīstības gaitu, tās pamatā esošie neirobioloģiskie faktori joprojām nav skaidri saprotami. Relatīvi mazā iespēja (~ 37%) to pārmantot, neskaidrība par to, kā būtiski ietekmēt depresijas risku, daudzveidīgie depresijas riska cēloņi un depresijas neviendabīgums tikai palielina grūtības identificēt ģenētiskos uzņēmības faktorus.
Tādi vides faktori kā trauma un strespilni dzīves notikumi palielina depresijas risku, mainot smadzeņu struktūru, ķīmiju un funkcijas. Hroniska sociālo, psiholoģisko vai fizisko stresa faktoru ietekme rada pētniecībai noderīgu vidi, lai saprastu, kā smadzenes transformē vides stresu par depresiju.
Depresijas un ar stresu saistītu traucējumu fiziopatoloģijas un ārstēšanas pamatā esošie mehānismi joprojām nav izprasti, taču pētījumi ar nomāktiem pacientiem un grauzējiem ir ļāvuši iegūt daudzsološus secinājumus. Šie pētījumi rāda, ka depresija un hronisks stress var izraisīt neironu atrofiju smadzeņu garozā un depresijā iesaistītajos limbiskajos smadzeņu reģionos, un smadzeņu attēlveidošanas pētījumos ir redzamas izmaiņas neironu tīkla savienojumos un smadzeņu funkcijās. Pētījumi par šo pārmaiņu neirobioloģisko pamatu pievēršas principam, ierosas glutamātu neironiem, gan kavējošajiem GABA interneironiem. Centrālās gamma-aminosviestskābes sistēmas disfunkcija jau izsenis ir saistīta ar trauksmes spektra traucējumiem. Lai gan salīdzinājumā ar glutamātu GABA neironi ir vismazākā daļa no kopējā neironu daudzuma (apmēram 15-20%), kavējošās neirotransmisijas un ierosas transmisijas līdzsvars ir būtisks normālai smadzeņu funkcijai.
Spriežot pēc liecībām par mainītu glutamātu un funkcionālo savienojamību, nav nekāds pārsteigums, ka ir liecības arī par pārtrauktu GABA neirotransmisiju, kas veicina VDT neiroloģisko ainu.
Īsumā, depresija bieži tiek saistīta ar GABAerģisko funkcijas samazināšanos, savukārt dažādas antidepresantu (AD) manipulācijas to šķietami palielina; pastāv pieņēmums, ka GABA funkcija ir pārmantots bioloģiskais marķieris, kas liecina par noslieci uz depresiju; pozitīviem GABA-A receptoru modulatoriem var būt AD iedarbība, savukārt negatīvi GABA-A modulatori bieži vien izraisa depresiju. Ir savākts liels pierādījumu kopums, kas apstiprina to, ka GABAerģiskie anksiolītiskie medikamenti pacientiem tik tiešām izraisa AD efektu.
Apkopojot iepriekš minēto, šķiet ticami, ka trauksmes un depresijas situācijā pārklājās GABAerģiskie mehānismi, jo tiem ir:
- kopīgi neiroķīmiskie mehānismi;
- līdzīgas smadzeņu struktūras, kas ir iesaistītas trauksmes un depresijas regulācijā;
- kopīga ģenētiska trauksmes un depresijas izcelsme; un
- pārklājoša vai korelējoša medikamentu neiropsihofarmakoloģiskā ietekme.
Vairākos pētījumos ir parādīta tieša korelācija starp galvenajiem depresīvajiem traucējumiem un būtiski pazeminātu GABA koncentrāciju smadzenēs. Tas nozīmē nevis to, ka GABA deficīts izraisa depresiju, bet gan ka tas spēlē būtisku lomu vispārējās depresijas, PMS, UDHS, bipolāro traucējumu, panikas, baiļu, mentālo bloku, trauksmaina prāta un trauksmes ārstēšanā. Ārsti šādos gadījumos bieži vien izraksta benzodiazepīnus, taču to lietošanas lielākais trūkums galvenokārt ir saistīts ar iespējamu atkarības veidošanos. GABA uztura bagātinātāji neizraisa atkarību un ir viena no uzturvielām, ko var izmantot, lai veicinātu atradināšanos no benzodiazepīniem.
Optimālā GABA deva ir atkarīga no vajadzības un konkrētā cilvēka. Parastā prettrauksmes deva pieaugušajiem ir no 500 līdz 5000 mg dienā, sadalot to vairākās devās.
- Tiek uzskatīts, ka alkohols atdarina GABA iedarbību uz smadzenēm, saistoties ar GABA receptoriem un kavējoši iedarbojoties uz neironu signāliem.
- GABA ir iesaistīta ne tikai GABAerģiskajos mehānismos, bet ir konstatēta arī citos perifērajos audos, tostarp zarnās, kuņģī, olvados, dzemdē, olnīcās, sēkliniekos, nierēs, urīnpūslī, plaušās un aknās, lai gan minētajos orgānos šī viela ir daudz mazākā koncentrācijā nekā neironos.
- GABA pirmoreiz tika sintezēta 1883. gadā, un to sākotnēji pazina tikai kā augu un mikrobu vielmaiņas produktu.
- GABA ir atrodama arī augos. Tā ir visvairāk sastopamā aminoskābe tomātu apoplastos. Iegūtie pierādījumi liecina, ka tam ir būtiska loma augu šūnu signālu saziņā.
- GABA tēja ir bezskābekļa vidē īpaši fermentētas tējas lapas, kurās ir uzkrājusies GABA. Šī tehnoloģija ir radusies Japānā.

Safrāna krokuss (Crocus sativus L.)
Safrāna krokusa (Crocus sativus L.) labvēlīgās īpašības tiek plaši izmantotas austrumu farmācijā, kuras arsenālā ir aptuveni 300 farmaceitisko preperātu ar šī auga ekstraktu. Safrāna krokusa aktīvo vielu ietekme uz smadzeņu darbību ir daudz pētīta - ir novērojumi, ka cilvēkiem, kuri izmanto safrāna krokusu, ir uzlabojusies smadzeņu darbība, atmiņa un maņu orgānu darbība.
Krokuss ir iekļauts 75 zemu augošu īrisu dzimtas (Iridaceae) augu sugu ģintī. Krokusu izcelsme meklējama Alpos, Dienvideiropā un Vidusjūras reģionā, un, pateicoties kausam līdzīgajiem ziediem, tas ir iecienīts pavasara vai rudens kultūraugs. Pavasarī uzziedējušajiem augiem ir gara ziedkopa, kas patur sēklotni zem zemes, pasargājot to no klimata pārmaiņām. Ziedi naktī un mākoņainā laikā aizveras. Krāsošanai, garšvielām un medikamentiem izmantotais safrāns tiek iegūts no violetā vai baltā, rudenī ziedošā safrāna krokusa (Crocus sativus) auglenīcas pūkainā gala. Safrāna krokuss rudenī parasti uzzied ar violetiem ziediem. Šis augs ir 10 līdz 30 cm garš.
Safrāns ir izkaltētas zili-violetā safrāna krokusa pagarinātās drīksnas un auglenīcas kāti. Safrāna drīksnas satur četras svarīgākās bioaktīvās sastāvdaļas: krokīnus (seši-monoglikozil- vai diglikozilpoliēna esteru grupa), kroketīnu (dabisks krokīna karotenoīda dikarboksilskābes prekursors), pikrokrokīnu (safrāna monoterpēna glikozīda prekursors un zeaksantīna noārdīšanās produkts) un safranālu. Pastāv pieņēmums, ka krokīns un safranāls kavē dopamīna, norepinefrīna un serotonīna atkaluzņemšanu.
Safrāns var uzlabot garīgo veselību, pateicoties tā antidepresanta īpašībām, un nesenā meta-analīzē tika apstiprināts, ka tas ir iedarbīgs depresijas ārstēšanas līdzeklis.
Uzņemot orāli: safrāns, visticamāk ir drošs tādos daudzumos, kas ir sastopams pārtikā un ja to lieto kā medikamentu kursa veidā ne ilgāk par 26 nedēļām. Dažas iespējamās blaknes ir sausa mute, trauksme, uzbudinājums, miegainība, nomākts garastāvoklis, slikta dūša vai vemšana, aizcietējumi vai caureja, apetītes izmaiņas, karstuma viļņi un galvassāpes. Dažiem cilvēkiem var rasties alerģiskas reakcijas.
Iespējams, ka safrāna lietošana lielās devās nav droša. Lielas devas, sākot no 5 gramiem vai vairāk, var izraisīt saindēšanos. 12-20 gramu lielas devas var izraisīt nāvi.
Grūtniecība un barošana ar krūti. Safrāna orāla lietošana devās, kas pārsniedz parasti produktiem pievienoto, visticamāk, nebūs droša. Lielākas safrāna devas var izraisīt dzemdes kontrakcijas un tādējādi – spontāno abortu.
Nav pietiekami daudz uzticamas informācijas, lai apgalvotu, ka safrāns ir drošs grūtniecēm vai ar krūti barojošām māmiņām. Labāk ievērojiet drošu pieeju un izvēlieties tādu daudzumu, kas parasti tiek pievienots pārtikai.
Bipolārie traucējumi. Safrāns var ietekmēt noskaņojumu. Pastāv bažas, ka tas var veicināt uzbudināmību un impulsīvu uzvedību (māniju) cilvēkiem, kas cieš no bipolārajiem traucējumiem. Nelietojiet safrānu, ja jums ir šāda diagnoze.
Alerģija pret airenēm, olīvkoku (tostarp olīvām) un kālija sālszāli: cilvēki, kam ir alerģija pret šiem augiem, varētu reaģēt alerģiski arī uz safrānu.
Mijiedarbība. Lietojot safrānu kā uztura bagātinātāju, piesardzība ir jāievēro cilvēkiem, kas lieto asinsspiediena regulēšanas un asins šķidrināšanas medikamentus. Ja lietojat medikamentus, pirms šī auga lietošanas konsultējieties ar ārstu.
Depresijas izraisīti traucējumi ir viena no dominējošajām garīgajām slimībām, un tiek lēsts, ka tā ietekmē līdz pat 21% pasaules iedzīvotāju. Vairums pacientu bieži vien nevēlas lietot sintētiskos antidepresantus ārstu izrakstītajās devās, jo tiem ir tādas blaknes kā nespēja vadīt automašīnu, sausa mute, aizcietējumi un libido zudums. Līdz ar to augu ekstrakti ir pievilcīgas jauno medikamentu alternatīvas, un ir pierādīts, ka depresijas ārstēšanā tie sniedz labāku rezultātu ar mazāk blaknēm.
Safrāna kā antidepresanta ieguvumi ir pietiekami dokumentēti. Veicot šī auga ķīmisko analīzi, tika iegūti gandrīz 150 gaistošie un negaistošie savienojumi. Līdz šim ir iegūtas un konstatētas mazāk par 50 sastāvdaļām ar fitoķīmiskajām īpašībām.
Ir secināts, ka krokīns un safrāna ekstrakts novērš hroniska stresa izraisītas atmiņas un telpiskās mācīšanās traucējumus. Pastāv pieņēmums, ka safrāna profilaktiskās īpašības, kas pasargā no atmiņas pasliktināšanās, ir saistītas ar safrāna antioksidanta īpašībām, kas labvēlīgi pretdarbojas oksidatīvā stresa izraisītajiem bojājumiem. Akhondzadeh et al., 2004. gadā veiktajā dubultmaskētajā un randomizētajā pētījumā, kas notika 6 nedēļu periodā, izdevās pierādīt, ka safrāna ekstrakta efektivitāte ir līdzvērtīga imipramīna iedarbībai. 6 nedēļu ilgušos dubultaklajos, randomizētajos klīniskajos pētījumos tika konstatēta arī kaltētu safrāna ziedlapiņu labvēlīgā ietekme uz vieglu līdz vidēji smagu depresiju. 4 nedēļas ilgs novērojums randomizētā, dubultmaskētā, daudzsološā eksperimentālajā klīniskajā pētījumā ar placebo grupu, piedaloties 40 galvenā depresīvā traucējuma pacientiem, safrāna drīksnu galvenā antioksidantu sastāvdaļas – krokīna – lietošana (30 mg/d) apliecināja selektīvo serotonīna atkaluzņemšanas inhibitoru iedarbības paplašināšanos ārstēšanā iekļautajiem pacientiem bez būtiskām blaknēm.
Cits pētījums (šajā dubultmaskētajā, placebo kontrolētajā un randomizētajā pētījumā pacientiem pēc nejaušības principa 6 nedēļas tika dota C.sativus ziedlapu kapsula 30 mg/dienā (BD) (1. grupa) un placebo kapsula (BD) (2. grupa)) parādīja, ka, dodot pacientiem ar vieglu līdz vidēji smagu depresiju C.sativus ziedlapu preparātu, pēc 6 nedēļu ārstēšanas tika panākti statistiski būtiski noskaņojuma uzlabojumi. Šo atklājumu klīnisko nozīmīgumu pastiprināja uzlabojumi pēc Hamiltona depresijas novērtējuma skalas punktiem safrāna grupā. Turklāt starp abām grupām novēroto blakņu ziņā nebija būtiskas atšķirības. Vismaz trijos no klīniskajiem pētījumiem ir iegūti dati, ka C.sativus drīksnām ir antidepresanta ietekme (Akhondzadeh et al., 2004, 2005; Noorbala et al., 2005).
- Safrāna krokuss smaržo līdzīgi vaniļai un garšvielām, un žāvētas drīksnas piešķir ēdienam, piemēram spāņu paeljai, rīsu ēdieniem un Vidusjūras zivju sautējumam, īpašu garšu.
- Safrāna vārda izcelsme ir meklējama franču valodas “safran”, kas atvasināts no latīņu vārda “safranum” – intensīvi dzeltens pigments; fitoķīmiskā analīze ir ļāvusi secināt, ka krāsu galvenokārt rada noārdījušies karotenoīdu savienojumi – krokīns un kroketīns.
- Safrāna drīksnas kā medikamentu sāka izmantot vairāk nekā pirms 3600 gadiem. Safrāns tika iekļauts dažādos opioīdajos preparātos, kurus izmantoja sāpju mazināšanai (16.-19. gs.). Safrānu arī izmantoja tuniku krāsošanai Spānijas reģionā un babiloniešu kultūrā apmēram 2400 pr. Kr.
- Tā ir pasaulē dārgākā garšviela ar mazumtirdzniecības cenu līdz pat 11 000 $/kg, jo tās iegūšana prasa daudz darba. Katram ziedam ir trīs sarkanas krāsas drīksnas, un viena safrāna drīksna sver apmēram 2 mg. Lai iegūtu 1 kg šīs unikālās garšvielas, ir nepieciešami 150 000 krokusa ziedi vai 450 000 ar rokām nolasītas drīksnas.
- 10 g vai lielāka deva var izraisīt abortu un cilvēkam letāla deva ir 20 g.
- Safrāns persiešu tradicionālajā medicīnā tiek izmantots depresijas ārstēšanai. Ir vērts pieminēt, ka tas ir persiešu garšaugs, kura vēsture ir tikpat sena kā Persijas Impērija.

Pasiflora (Passiflora incarnata L.)
Pasiflora (Passiflora incarnata L.) ir daudzgadīgs augs, kas var izaugt līdz pat 10 m augstumam ar ovāliem, ēdamiem augļiem.Ēdamo pasifloru mēs pazīstam kā marakuju. Dabā šos spilgtos, eksotiskos ziedus var sastapt Austrālijā, Āzijā un Dienvidamerikā(Brazīlijā). Šim augam ir nomierinoša iedarbība uz nervu sistēmu;tas spēj regulēt miega traucējumus; stabilizē asinsspiedienu un uzlabo asinsriti. Visas šīs īpašības ir saistītas ar pasifloras ziedu sastāvu, kurš satur flavonoīdus, brīvos fenola savienojumus, glikozīdus, kā arī organismam svarīgas aminoskābes un virkni organisko skābju, tai skaitā: ābolskābi, skudrskābi, linolskābi un citas.
Pasifloru (Passiflora incarnata L.) jeb kaisles ziedu - kultivē, lai iegūtu izejvielas farmācijas vajadzībām. Passiflora incarnata ir viena no vislabāk dokumentētajām Pasifloras ģints sugām ar ārstnieciskām īpašībām. Medicīniskiem nolūkiem tiek izmantots gan viss augs, gan ziedi un augļi.
Pasifloras vērtīgās īpašības un blakusparādības, to lietojot, ir pētītas jau sen dažādu zāļu preparātos. Ņemot vērā, ka šim augam piemīt unikālas farmakoloģiskas īpašības, tā popularitāte pēdējā laikā pieaug.
Pasiflora ir alkaloīdu, fenola savienojumu, flavonoīdu un cianogēno glikozīdu avots. Pasifloras primārās fitoķīmiskās vielas ir flavonoīdi (apigenīns, luteolīns, kvercetīns un kaempferols) un flavonoīdu glikozīdi (viteksīns, izoviteksīns, orientīns un izoorientīns).1
C-glikozilētie flavonoīdi un izoviteksīns, kas atrodami pasiflorā, modulē GABAA receptorus, izmantojot savas benzodiazepīnu saistīšanās vietas un vienlaicīgi rada anksiolītiskiem līdzekļiemraksturīgu ietekmi un kognitīvās (izziņas) uzlabošanās efektu.2
2014. gada 25. martā Eiropas Zāļu aģentūra publicēja augu monogrāfiju par Passiflora incarnata, tādējādi atzīstot tai zāļu statusu.3
Passiflora incarnata ir svarīga trauksmes vai nervozitātes, ģeneralizētas trauksmes, opiātu abstinences simptomu, bezmiega, neiralģijas, krampju, spazmas astmas, UDHS, sirdsklauves, sirds ritma anomāliju, hipertensijas, seksuālās disfunkcijas un menopauzes augu izcelsmes medicīniskajā ārstēšanā.
Neskatoties uz mūsu izpratnes nepilnībām par neirofizioloģiskajiem procesiem, arvien vairāk tiek atzīts, ka neiropsihiski stāvokļi, kas saistīti ar depresiju un trauksmi centrālajā nervu sistēmā, attiecas uz līdzsvaru starp ķīmisko ierosmi un inhibīciju. Viens no mehānismiem ir saistīts ar γ-aminosviestskābes (GABA) sistēmu.4Tāpēc tika pētīta Passiflora incarnata sausā ekstrakta ietekme uz GABA sistēmu in vitro. Pētījumi parādīja, ka daudzas Passiflora incarnata farmakoloģiskās iedarbības ir saistītas ar GABA sistēmas modulāciju, tostarp afinitāti (vielas īpašība veidot savienojumu ar citu vielu) pret GABAA un GABAB receptoriem un ietekmi uz GABA uzņemšanu. Pasiflorā esošo polifenolu un flavonu anksiolītiskās aktivitātes var daļēji saistīt ar to pretkairinājuma un antioksidantu iedarbību to specifisko struktūru dēļ. Turklāt pierādītas ievērojams skaits šo savienojumu anksiolītiskās īpašības, aktivizējot GABAA receptorus.
Lietojot pasifloru saturošus produktus reizēm ir novērojamasblakusparādības. Biežākās blakusparādības ir:
- • reibonis;
- • miegainība;
- • apjukums;
- • slikta dūša;
- • vemšana;
- • pazemināts asinsspiediens;
- • patoloģiska sirdsdarbība un ritms.
Pasiflora jālieto piesardzīgi, ja Jūs jau lietojat kādu sedatīvumedikamentu, piemēram, alprazolāmu (Xanax), lorazepāmu (Ativan), temazepāmu (Restoril) un zolpidēmu (Ambien), jo lietojot tos vienlaicīgi ar pasifloru, palielinās pārmērīgas miegainības un sedācijas risks.
Pasiflora jālieto piesardzīgi kopā ar asinsspiediena zālēm, piemēram, enalaprilu (Vasotec), losartānu (Cozaar), atenololu (tenormīnu), amlodipīnu (Norvasc) un furosemīdu (Lasix). Pasiflorai ir asinsspiedienu pazeminoša iedarbība un, lietojot asinsspiediena zāles savienojumā ar pasifloru, assinspiediens var samazināties vairāk par nepieciešamo.
Ja Jūs lietojat kādus medikamentus un Jums ir radušies jautājumi par šo medikamentu savietojamību ar pasifloru, pirms šī produktalietošanas konsultējieties ar savu ārstu.
Pasifloru nav ieteicams lietot grūtniecēm un sievietēm, kuras baro bērnu ar krūti.
Stress ir dabiska ķermeņa reakcija. To var izraisīt fiziski (izsalkums, slāpes, infekcija) un/vai psiholoģiska rakstura faktori (saskatītidraudi, trauksme vai bažas), proti, stresa faktori. Stress ir saistīts ar šūnu kairinājumu. Fizioloģiski ķermeņa reakcija uz stresu izraisa tūlītēju adrenerģiskās sistēmas un simpātiskās-adrenomedulārās ass (SAM ass) aktivizēšanos, kam seko hipotalāma-hipofīzes-virsnieru ass (HPA ass). Hronisks, ilgstošs stress ir patoloģisks stāvoklis, kas var pasliktināt koncentrēšanos un atmiņu, kā arī izraisīt afektīvus traucējumus, piemēram, depresiju, šizofrēniju un pēctraumatiskā stresa traucējumus. Passiflora incarnata ir viens no augu izcelsmes līdzekļiem, ko izmanto, lai mazinātu stresa sekas. Žurku pētījumspierādīja, ka ilgstoša pasifloras lietošana ir saistīta ar samazinātu stresa līmeni un līdz ar to palielinājās motivācija rīkoties un uzlabojās motoriskā aktivitāte. Tāpat ir apstiprinājusies pasifloras labvēlīgā ietekme uz atmiņas funkciju.
Stress var ietekmēt miega kvalitāti un izraisīt bezmiegu. Pasifloraslietošana cilvēkiem ar hronisku bezmiegu var radīt terapeitisku efektu miega traucējumu, atmiņas zuduma un deģeneratīvas smadzeņu slimības gadījumā. Pasiflora, nomierinošās iedarbības dēļ, var būt noderīga arī trauksmes, nemiera, bezmiega un depresīvos stāvokļos.1
Lielākoties lietotās zāles trauksmes ārstēšanai ietver benzodiazepīnu un buspirona anksiolītiskus līdzekļus, kā arī dažādusantidepresantus, kuri var izraisīt blakusparādības un panesamības problēmas.
Pētījumā2, kurā tika izvirzīta hipotēze, ka orāli lietota Passiflora incarnata būtu efektīvs anksiolītisks līdzeklis ar ierobežotu ietekmi uz anestēziju un atveseļošanos, tika pierādīta pasifloras (500 mg) ietekme uz trauksmi pacientiem pirms operācijas. Secinājums:ambulatorajā ķirurģijā perorāla Passiflora incarnata lietošana kāpremedikācija samazina trauksmi, neizraisot sedāciju (miegainību).
Passiflora incarnata pie 500 mg/dienā nodrošina drošu un efektīvu anksiolītisku efektu, nepasliktinot psihomotorās funkcijas.

L-teanīns (L-Theanine)
L-teanīns (γ-glutamiletilamīds) ir unikāla bezproteīna aminoskābe,kas atrodama augos un sēnēs, kā arī zaļajā tējā (Camellia sinensis L.). L-teanīns palīdz mazināt trauksmi un veicina relaksāciju bez miegainības. Turklāt stresa reducēšanas efekts, lietojot L-teanīnu, irnovērots ne tikai kā subjektīvā stresa uztvere, bet arī fizioloģiskā stresa gadījumā (sirdsdarbības normalizēšana, siekalu izdalīšanās kontrole).
L-teanīns (γ-glutamiletilamīds) ir L-glutamīnskābes atvasinājums, aminoskābe, kas visvairāk asociējas ar tējas lapām (Camellia sinensis L.). Tam ir līdzīga ķīmiskā struktūra kā glutamātam(neiromediators, kas ir saistīts ar vairāk nekā 90 % no visiem sinapsiskajiem savienojumiem cilvēka smadzenēs). Nonākot galvas smadzenēs, L-teanīns pārvēršas par aktīvu neiromediatoru, kas nodrošina starpšūnu nervu impulsu pārvadi un efektīvi ietekmē kavēšanas un relaksācijas procesus. Jeb citiem vārdiem, Jūsu garastāvokli, koncentrēšanos, miega režīmu, apetīti un modrību galvenokārt ietekmē dažādi neiromediatori - endogēnas ķīmiskas vielas, kas caur sinapsi, pārraida signālu no neirona uz mērķa šūnu, tostarp GABA (gamma-amino sviestskābe), serotonīns un dopamīns, kā arī smadzeņu darbību inhibējošie (kavējošie) hormoni, piemēram, kortizols un kortikosterons. Kad esat pakļauts stresam, paaugstinās kortizola un kortikosterona līmenis, kā rezultātā samazinās smadzeņu darbība.1
Lai to novērstu L-teanīns pastiprina neiromediatoru darbību,piemēram, GABA, tādējādi samazinot smadzeņu uzbudinošo ķīmisko vielu - kortizola un kortikosterona, - līmeni un veicina relaksāciju. Paaugstināts kortizola un kortikosterona līmenis ne tikai rada trauksmi, bet ietekmē arī dažādas citas smadzeņu darbības, piemēram, telpisko mācīšanos un atmiņu.
Šobrīd ir zināmi četru veidu elektromagnētiskie viļņi cilvēka smadzenēs: beta, alfa, teta un delta viļņi. Katram no tiem ir raksturīgs savs frekvences diapazons un katrs no tiem tiek saistīts ar atšķirīgu darbību, piemēram, teta viļņi ir saistīti ar miegainību, bet alfa viļņi - ar atslābināšanos. Alfa smadzeņu viļņi tiek uzskatīti par atslābināšanās jeb relaksācijas mērauklu. To darbība ir saistīta ar paaugstinātu radošumu, labākiem sniegumiem stresa apstākļos, veiksmīgākām mācīšanās un koncentrēšanās spējām, kā arī samazinātu trauksmi. L-teanīns palielina alfa viļņu aktivitāti, tādējādi atslābinot smadzeņu darbības aktivitāti.1; 2 Turpinot atslābināties, alfa viļņi sāk dominēt visās galvas smadzenēs. Šo viļņu trūkumu izraisa stress, slimības, nemiers.
L-teanīna lietošana parasti tiek uzskatīta par drošu. Tas nav saistīts ar nopietnu nelabvēlīgu ietekmi.
Biežākās L-teanīna lietošanas blakusparādības ir galvassāpes, slikta dūša un aizkaitināmība.1 Tomēr šķiet, ka slikta dūša galvenokārt ir saistīta ar L-teanīna lietošanu, lietojot zaļo tēju, nevis uztura bagātinātājus. Līdzīgi aizkaitināmības blakusparādība ir saistīta ar kofeīna un L-teanīna dubultu lietošanu.
Ja Jūsu ierastā atbilde uz jutājumu “Kā tev iet?” ir “Saspringti - darbs dzen darbu” vai “Neko nevaru paspēt”, iespējams, vēlēsieties ikdienas gaitas papildināt ar L-teanīnu, lai mazinātu Jūsu stresa un trauksmes simptomus.1
L-teanīns ir saistīts ar prettrauksmes iedarbību, kavējot kortikālo neironu ierosmi. Stress ir dabīga mūsu organisma reakcija uz briesmām. Piemēram, ieraugot mežā lāci, aktivizējas Jūsu simpātiskā nervu sistēma, izdalās hormoni, paātrinās sirdsdarbība, svīst rokas, mute paliek sausa utt. Tomēr Jūs varat aktivizēt savu simpātisko nervu sistēmu arī nejauši, tā teikt, “bez vajadzības”, un tā var kļūt par problēmu.
Labākajā gadījumā stresa ietekmes dēļ var būt nepatīkamas, sasvīdušus plaukstas. Sliktākajā gadījumā Jūs varat ciest no hroniska stresa un ar to saistītām fizioloģiskajām reakcijām, piemēram, paātrinātas sirdsdarbības un asinsspiediena paaugstināšanās vainovājinātu imunitāti.
Arī studenti ir pakļauti regulāram stresam. Stresa ietekmē paaugstinās kortikosterona hormona līmenis, un tā rezultātā smadzenes nespēj darboties tā, kā paredzēts. Līdz ar to mācīšanās kļūst neefektīva. Pētījumā2 tika pierādīts, ka lietojot L-teanīnu, tika nodrošināts ātrāks vienkāršas reakcijas laiks, ātrāks ciparu darba atmiņas reakcijas laiks un uzlabota teikumu pārbaudes precizitāte. Tādi personu pašvērtējumi kā “galvassāpes” un “nogurums” tika samazināti.
Tas pierāda, ka, samazinot hormona kortikosterona līmeni, L-teanīns aizsargā kognitīvās spējas no iespējamiem traucējumiem, kas varētu rasties augsta stresa hormona līmeņa dēļ.
Pētnieki ir konstatējuši3, ka L-teanīns palīdz regulēt augstu asinsspiedienu, palīdzot cilvēkiem stresa situācijās to uzturēt veselīgā līmenī.
Gadījumā, ja Jūs ciešat no stresa izraisīta bezmiega, L-teanīns var palīdzēt. Pētnieku komanda veica pētījumu4, lai izpētītu L-teanīna miega kvalitātes uzlabošanas spējas. Pētījums liecina, ka 200 mg L-teanīna lietošana pirms gulētiešanas uzlabo miega kvalitāti, nevis sedāciju, bet anksiolīzi. Tā kā L-teanīns neinducē dienas miegainību, tas var būt noderīgs lietošanai jebkurā diennakts laikā.
L-teanīna miega kvalitātes uzlabošana notiek dažādos veidos. Pirmkārt, aminoskābe liek cilvēkam labāk atpūsties un kļūt mazāk satrauktam. Ar relaksācijas stimulu un samazinātu stresu aizmigšana notiek vieglāk un ātrāk. Samazinot trauksmi un veicinot relaksāciju, L- teanīns palīdz iziet visu parasto miega ciklu, ieskaitot tik ļoti nepieciešamo dziļo REM fāzi, lai panāktu pilnīgu prāta un ķermeņa atsvaidzināšanu.

B6 vitamīns
B6 vitamīns, dēvēts arī par piridoksīnu, piedalās aminoskābju un tauku vielmaiņā. Šī vitamīna trūkums rada anēmiju, nespēku, depresiju vai nervozitāti, kā arī ādas iekaisumu. B6 vitamīns sekmē sarkano asinsķermenīšu un hemoglobīna veidošanos.
B6 vitamīns (piridoksīns) tika atklāts 1934. gadā. Tā ir ūdenī šķīstoša viela, kas organismā pārvēršas par svarīgākajiem koenzīmiem. B6 vitamīns koenzīma formās pilda dažādas funkcijas organismā un ir ārkārtīgi daudzpusīgs, iesaistoties vairāk nekā 100 enzīmu reakcijās, kas galvenokārt saistītas ar olbaltumvielu metabolismu (vielmaiņu).
B6 vitamīnam ir trīs dabiskās formas: piridoksīns, piridoksāls un piridoksamīns, un tās visas organismā pārvēršas aktīvās formās, kas ir koenzīms piridoksāla 5-fosfāts (PLP vai P5P). PLP galvenokārt kalpo kā koenzīms aminoskābju, olbaltumvielu, ogļhidrātu un lipīdu metabolismā, papildu neirotransmiteru (bioloģiski aktīvas vielas, kas sintezējas neironā un izdalās sinapsē; saistoties ar citas šūnas receptoriem, tie pārnes nervu impulsu no sinapses uz šūnu) sintēzei.Tas ir iesaistīts arī glikogenolīzē un glikoneoģenēzē.1
Piridoksīns, piridoksamīns un piridoksāls ātri uzsūcas no pārtikas un iekšķīgi lietojamām zālēm un uztura bagātinātējiem tievās zarnas gļotādas šūnās, savukārt to fosforilētie analogi vispirms tiek defosforilēti un uzsūcas pēc tam.
B6 vitamīnam ir nozīmīga un selektīvi modulējoša ietekme uz centrālo serotonīna un GABA veidošanos2. GABA ir smadzenēs atrodama ķīmiska viela un inhibējošs neirotransmiters. Par GABA vairāk lasi šeit. Tas palīdz nomierināt nervu sistēmu, bloķējot noteiktus impulsus starp nervu šūnām, palēninot smadzeņu darbību, attiecīgi, tam ir nomierinoša iedarbība, kas var palīdzēt mazināt stresu, trauksmi un bailes.
Bioķīmiski, daļēja B6 vitamīna deficīta gadījumā, daži enzīmi var tikt ietekmēti vairāk nekā citi, izraisot lielāku dažu neirotransmiteru darbības vājināšanos un tādējādi izjaucot līdzsvarotību starp dažādiem neirotransmiteru līmeņiem.3 Attiecīgi, izraisot tādus neiroloģiskos traucējumus kā kognitīvo funkciju pasliktināšanās, konvulsīvus krampjus, depresiju un pat priekšlaicīgu neironu novecošanos (CNS ietekme).
Tātad, svarīgākā B6 vitamīna funkcija - tas darbojas kā koenzīms nepieciešamo neirotransmiteru sintēzē sinaptiskajai transmisijai (piemēram, dopamīns, serotonīns, GABA) un veic neiroprotektīvulomu, pamatojoties uz tās nozīmi glutamaterģiskajā sistēmā.
Trūkums organismā un uzņemšanas avoti
B6 vitamīna deficītu klīniski var novērot kā seborejas dermatītu, mikrocītu anēmiju, zobu bojāšanos, glosītu, epileptiformas krampjus, perifēro neiropātiju, elektroencefalogrāfiskas novirzes, depresiju, apjukumu un novājinātu imūno funkciju.1
B6 vitamīna deficīts ir salīdzinoši reti sastopams, taču dažiem cilvēkiem B6 vitamīna līmenis var būt samazināts.
Cilvēki, kuriem varētu būt samazināts B6 vitamīns:
Cilvēkiem ar nepilnvērtīgu nieru darbību, tostarp tiem, kuriem ir hroniska nieru mazspēja, kuri saņem uzturošo nieru dialīzi, kuriem ir veikta nieres transplantācija, bieži ir zems B6 vitamīna līmenis.
Cilvēkiem ar reimatoīdo artrītu bieži ir zems B6 vitamīna līmenis asinīs un šim līmenim ir tendence samazināties, palielinoties slimības smagumam. Šis zemais B6 vitamīna līmenis ir saistīts ar slimības izraisīto iekaisumu. Lai gan pacientiem ar reimatoīdo artrītu B6 vitamīna papildus lietošana var normalizēt B6 vitamīna koncentrācijuasinīs, taču tā nenomāc iekaisuma citokīnu veidošanos un nesamazina iekaisuma marķieru līmeni.
Pacientiem ar celiakiju, Krona slimību, čūlaino kolītu, iekaisīgu zarnu slimību un citiem malabsorbcijas autoimūniem traucējumiem parasti ir zems vitamīna B6 līmenis.
Cilvēkiem, kuri ir atkarīgi no alkohola, B6 vitamīna koncentrācija plazmā mēdz būt ļoti zema. Alkohols ražo acetaldehīdu, kas samazina neto B6 veidošanos šūnās un konkurē ar piridoksāla 5-fosfātuproteīnu saistīšanā. Rezultātā piridoksāla 5-fosfāts šūnas var būt jutīgākas pret hidrolīzi, ko veic ar membrānu saistītā fosfatāze. Cilvēkiem ar alkohola atkarību būtu ieteicams regulāri uzņemt vitamīna B6 piedevas.
Pieaugušiem cilvēkiem, kuriem nav novērots vai apstiprināts B6 vitamīna deficīts, normāli ir nepieciešams 1,3 mg (grūtniecēm 2 mg) B6 vitamīna dienā.
Nav ziņots, ka liela B6 vitamīna uzņemšana no pārtikas avotiem izraisītu nelabvēlīgu ietekmi, tomēr ilgstoša 1–6 g perorāla piridoksīna lietošana dienā 12–40 mēnešus var izraisīt smagu un progresējošu sensoro neiropātiju. Perifēro nervu šķiedru un to mielīna, kā arī muguras smadzeņu kanālu deģenerācija izraisa abpusēju perifērās sajūtas zudumu vai hiperestēziju, ko pavada sāpes ekstremitātēs, ataksija (kustību koordinācijas un līdzsvara traucējumi)un līdzsvara zudums. Stāvoklis pakāpeniski regresē pēc papildusvitamīna B6 lietošanas pārtraukšanas līdz normālas aktivitātes atjaunošanai.1 Lielākas devas var izraisīt sēklinieku atrofiju un samazināt spermatozoīdu kustīgumu.
Mijiedarbība ar medikamentiem
B6 vitamīns var mijiedarboties ar noteiktiem medikamentiem un vairāki medikamentu veidi var negatīvi ietekmēt B6 vitamīna līmeni. Minēsim dažus piemērus. Personām, kuras regulāri lieto šīs un citas zāles, jāapspriež sava B6 vitamīna lietošana ar saviem veselības aprūpes sniedzējiem.
Cikloserīns (Seromycin®) ir plaša spektra antibiotika, ko lieto tuberkulozes ārstēšanai. Kombinācijā ar piridoksāla fosfātu cikloserīns palielina piridoksīna izdalīšanos ar urīnu. Piridoksīna izdalīšanās urīnā var saasināt krampjus un neirotoksicitāti, kas saistīta ar cikloserīnu. Piridoksīna papildus uzņemšana var palīdzēt novērst šīs nelabvēlīgās sekas.
Dažas pretepilepsijas zāles, tostarp valproiskābe (Depakene®, Stavzor®), karbamazepīns (Carbatrol®, Epitol® un citi) un fenitoīns (Dilantin®) palielina B6 vitamīna katabolisma(vielmaiņas procesu kopums, kas sadala molekulas mazākās vienībās, kuras tiek oksidētas, lai atbrīvotu enerģiju) ātrumu, kā rezultātā samazinās B6 koncentrācija un var attīstīties hiperhomocisteinēmija. Augsts homocisteīna līmenis pretepilepsijas līdzekļu lietotājiem var palielināt epilepsijas lēkmju un, tostarp, insulta risku un samazināt spēju kontrolēt krampjus. Turklāt pacienti parasti lieto pretepilepsijas līdzekļus gadiem ilgi, palielinot hroniskas asinsvadu toksicitātes risku.
Teofilīns (Aquaphyllin®, Elixophyllin®, Theolair®, Truxophyllin® u.c.) var novērst vai ārstēt elpas trūkumu, sēkšanu un citas elpošanas problēmas, ko izraisa astma, hronisks bronhīts, emfizēma un citas plaušu slimības. Ar teofilīnu ārstētiem pacientiem bieži ir zema B6 vitamīna koncentrācija plazmā, kas var veicināt ar teofilīnu saistītās neiroloģiskas un centrālās nervu sistēmas blakusparādības, tostarp,krampjus.
Jaunākajos pētījumos pētnieki ir meklējuši saistību starp garastāvokļa traucējumiem, piemēram, depresiju un trauksmi, stresu un B6 vitamīna lietošanu. Piemēram, astoņas nedēļas ilgs IV fāzes randomizēts kontrolēts pētījums atklāja, ka magnija un B6 vitamīna kombinācija spēj nodrošināt lielāku fizisko aktivitāti ikdienas dzīvē un ievērojamu stresa samazināšanos veseliem cilvēkiem ar smagu stresu un trauksmi un zemu magnija līmeni.1
Ņemot vērā dažādu pētījumu rezultātus, var secināt, ka B6 vitamīns aktīvi palīdz mazināt simptomus, kas raksturīgi depresijai un trauksmei, padarot šo vitamīnu par svarīgu ikdienas dzīves papildinājumu. Vēl viens svarīgs apsvērums par labu B6 vitamīnam ir tas, ka, lai gan benzodiazepīni (piemēram, diazepāms, fenazepāmsu.c.) ir efektīvi trauksmes un citu līdzīgu stāvokļu ārstēšanā, tiem ir arī vairākas blakusparādības, tostarp, bet ne tikai, atkarība, atsitiena trauksme, atmiņas traucējumi un lietošanas pārtraukšanas sindroms.

L-tirozīns (L-tyrosine)
L-tirozīns ir aizvietojama aminoskābe, ko organisms ražo no citas aminoskābes, ko sauc par fenilalanīnu. L-tirozīns ir iesaistīts vairāku svarīgu smadzeņu ķīmisko vielu, kas palīdz nervu šūnām sazināties (neirotransmiteru), ražošanā, tostarp epinefrīna, norepinefrīna un dopamīna. L-tirozīns arī palīdz ražot melanīnu, pigmentu, kas atbild par matu un ādas krāsu. Tas palīdz to orgānu darbībā, kas ir atbildīgi par hormonu veidošanos un regulēšanu, tostarp virsnieru dziedzeri, vairogdziedzeri un hipofīzi. Tas ir iesaistīts gandrīz visu ķermeņa olbaltumvielu struktūrā. Zems L-tirozīna līmenis ir saistīts ar pazeminātu asinsspiedienu, zemu ķermeņa temperatūru un nepietiekamu vairogdziedzera darbību.
L-tirozīns ir aizvietojama aromātiskā aminoskābe, kas organismā kalpo kā izejviela dažādu citu vielu sintēzei, piemēram, tā ir priekštecis tiroīdā hormona tiroksīna (T4) (rodas, jodējot tirozīnu), pigmenta melanīna un citu tādu bioloģiski aktīvu vielu sintēzei kā kateholamīniem - epinefrīnam (adrenalīns), norepinefrīnam(noradrenalīns) un dopamīnam. Šīs ir ļoti svarīgas bioloģiski aktīvasvielas, kas sintezējas neironā un izdalās sinapsē; saistoties ar citas šūnas receptoriem, tās pārnes nervu impulsu no sinapses uz šūnu (neirotransmiteri), kas ir cieši saistītas ar atbilstošu L-tirozīna koncentrāciju organismā.
L-tirozīns ietilpst daudzu dabisko olbaltumvielu, tai skaitā fermentu, sastāvā. Organismā L-tirozīns sintezējas no fenilalanīna ar fermenta fenilalanīn-4-hidroksilāzes palīdzību.
Kā tirozīns darbojas mūsu organismā? Pirmkārt, vairogdziedzeris no pārtikas absorbē jodu. Kad šīs joda molekulas ir oksidētas, tās ir gatavas pievienoties tirozīnam, kas atrodas tiroglobulīnā (proteīns, ko ražo vairogdziedzeris). Kad jods un tirozīns savienojas, tie rada vairogdziedzera hormona prekursorus, monojodtirozīnu (T1) un dijodtirozīnu (T2). Pēc tam T1 un T2 apvienojas, veidojot vairogdziedzera hormonus trijodtironīnu (T3; tiroglobulīns ar trim joda molekulām) un tiroksīnu (T4, tiroglobulīns ar četrām joda molekulām). T4 un T3 ir primārie vairogdziedzera hormoni, kas ir būtiski vielmaiņas procesu regulēšanai visā organismā.
Tātad, apkopojot tirozīna lomas organismā, jāmin šādas:
Tirozīna trūkums var izraisīt vairogdziedzera disfunkciju, piemēram, hipotireozi, kā arī izraisīt depresiju vai pastiprinātu nervozitāti dēļ traucētās kateholamīnu sintēzes.
L-tirozīns ir uzskatāms kā drošs lielākajā daļā devu, taču pirms tā lietošanas tomēr vajadzētu konsultēties ar savu ārstu, ja lietojiet kādus medikamentus. Tas var mijiedarboties ar zālēm, tostarp dažām zālēm, ko lieto vairogdziedzera darbības traucējumu vai depresijas ārstēšanai.
Monoamīnoksidāzes inhibitori (MAOI) – tirozīns var izraisītnopietnu asinsspiediena paaugstināšanos cilvēkiem, kuri lieto antidepresantus, kas pazīstami kā MAOI. Šī straujā asinsspiediena paaugstināšanās, ko sauc arī par "hipertensīvo krīzi", var izraisīt sirdslēkmi vai insultu. Cilvēkiem, kuri lieto MAOI, vajadzētu izvairīties no pārtikas un uztura bagātinātājiem, kas satur tirozīnu. Piemēram:
Levodopa - tirozīnu nedrīkst lietot vienlaikus ar levodopu, medikamentu, ko lieto Parkinsona slimības ārstēšanai. Levodopa var traucēt tirozīna uzsūkšanos.
Atsevišķos gadījumos tirozīna papildus lietošana var izraisīt bezmiegu, nemieru, sirdsklauves, galvassāpes, kuņģa darbības traucējumus un grēmas.
Tā kā tirozīns ir iesaistīts vairogdziedzera hormonu ražošanā, to nedrīkstat lietot, ja ir diagnosticēta vairogdziedzera slimība, piemēram, hipertireoze vai Greivsa slimība.
Tirozīna ieteicamā diennakts deva, ko uzņemam ar uzturu (IDD), ir 25 mg uz kilogramu ķermeņa svara.1 Pieņemot, ka cilvēks saņem pusi no nepieciešamās aminoskābes, sanāk 12,5 mg uz kg. Tādējādi personai, kas sver 70 kg, dienā vajadzētu patērēt aptuveni 875 mg tirozīna, un tas ir daudzums, ko izmanto, lai aprēķinātu IDD. Tirozīns ir atrodams dažādos pārtikas produktos, piemēram, zemesriekstos, zivīs, vistas gaļā, tītarā, sojā, olās un biezpienā. Tas ir arī ķirbju sēklās, auzās, kviešos, pupās, sezama sēklās, avokado un banānos.
Hipotireoze jeb pavājināta vairogdziedzera funkcija nozīmē, ka vairogdziedzeris nepietiekošā daudzumā izstrādā svarīgus hormonus, kuriem ir ietekme uz visiem vielmaiņas procesiem. Biežākie hipotireozes cēloņi ir hronisks autoimūns tireoidīts, dažādu medikamentu lietošana, staru terapija un vairogdziedzera operācijas. Jāņem vērā arī apstāklis, ka cilvēki nelabprāt savā uzturā lieto jūras dārzeņus, piemēram, brūnaļģes, kā arī garšas dēļ cilvēki lapbprātāk izvēlas sāli bez joda piedevas, kas arī ir iemesls tam, ka joda trūkums kļūst arvien izplatītāks.
Biežākie hipotireozes simptomi ir nogurums, paaugstināta jutība pret aukstumu, sausa āda, trausli mati, cilvēks izskatās daudz vecāks nekā ir faktiski. Sievietēm bieži ir neregulāras menstruācijas, kognitīvie traucējumi, depresija.
Ir arī pierādīts, ka cilvēkiem, kuriem ir vairogdziedzera slimība, neatkarīgi vai tā būtu hipertireoze vai hipotireoze, ir ļoti svārstīgs tirozīna līmenis asins serumā, un tiem, kuriem ir hipotireoze (zems vairogdziedzera hormonu līmenis), tirozīna līmenis asinīs parasti ir zemāks par normu.
Apvienojot to ar pierādīto faktu, ka medikamentu (piemēram, kuru sastāvā aktīvā viela ir levotiroksīns, sintētisks vairogdziedzera hormons, ko lieto vairogdziedzera slimību un darbības traucējumu ārstēšanai) lietošana uzlabo tirozīna metabolismu aknās, iespējams ir vērts konsultēties ar ārstu un apsvērt iespēju ikdienu papildināt gan ar vairogdziedzera zālēm, gan ar tirozīnu (vai ievērojot īpašu diētu, vai izmantojot uztura bagātinātājus).
Ja Jūs izvēlaties savu ikdienu papildināt ar L-tirozīnu, jāatceras, ka efektīvāk to ir lietot kopā ar citiem minerāliem, kas var uzlabot vairogdziedzera darbību, piemēram, cinku un selēnu. Cinks palīdz uzlabot tiroksīna (T4) pārveidi par trijodtironīnu (T3) hipotireozes pacientiem, kuriem ir nepietiekama vairogdziedzera funkcija.Savukārt, selēns palīdz samazināt vairogdziedzera antivielas, kā arī ir iesaistīts T4 pārveidošanā par T3.

Brūnaļģe (Fucus vesiculosus L.)
Brūnaļģe Fucus vesiculosus saukta par pūšļu fuku jeb pūšļaļģi, ir viena no izplatītākajām un svarīgākajām biotopu veidojošām sugām Baltijas jūrā. Brūnaļģe satur vairāk vitamīnu un minerālvielu nekā jebkurš cits pārtikas produkts. Minerālvielu daudzums ir viens no lielākajiem visos zināmajos augu avotos un Fucus vesiculosus trīs galvenās sastāvdaļas ir jods, algīnskābe un fukoidāns.
Fucus vesiculosus starp 66 sugu brūnaļģēm ir viena no ievērojamākajām Arktikas reģiona seklajos ūdeņos - Atlantijas okeānā, Klusā okeāna ziemeļu daļā, Barenca, Baltās, Norvēģijas, Baltijas un Irmingera jūrās. Šīs aļģes dominē sekla ūdens makroaļģu populācijās 0,5–4 m dziļumā jūras ūdeņos. Tās izmanto ne tikai pārtikā, bet arī kosmētikā, bioloģiskajos mēslošanas līdzekļos, dzīvnieku barībā un farmācijas rūpniecībā.1
Fucus vesiculosus sastāvā ir virkne veselību veicinošu savienojumu, piemēram, fukoidānu, polifenolu, fukoksantīna un būtisku minerālvielu avots, tostarp joda, kam ir laba biopieejamība, un selēna, kam ir galvenā nozīme vairogdziedzera darbības regulēšanā.Brūnaļģes ir īpaši bagātas ar jodu un tās tiek izmantotas kā dabīgs joda avots, kas organiski iekļaujas šūnu vielmaiņā.
Brūnaļģēs sastopamā algīnskābe (līdz 35 % no sausas masas) ir pazīstama pārtikas rūpniecībā. Tā kalpo par sastāvdaļu zupās un zupu maisījumos kā emulgators, biezinātājs un stabilizators.Savukārt, alginātu (algīnskābes sāļi) bāzes preparāti tiek izmantoti, lai ārstētu grēmas un kuņģa skābes refluksu (atvilni).2 Algīnskābe stimulē fagocitozi, tādējādi palielinot šūnu pretmikrobu, pretvīrusu un pretsēnīšu aktivitāti; saista lieko imūnglobulīnu E daudzumu, kuru dēļ attīstās alerģija; veicina imūnglobulīnu A (antivielu) sintēzi, kas palielina ķermeņa izturību pret mikrobiem. Tāpat, pateicoties algīnskābei, Fucus vesiculosus pazemina asinsspiedienu, noņem kaitīgos radionuklīdus un smagos metālus un vājina ķermeņa intoksikāciju.
Vēl viena svarīga Fucus vesiculosus sastāvdaļa ir fukoidāni. Fukoidāni ir polisaharīdi no Fucus saimes - savienojumi, kas ir unikāli brūnajām aļģēm. Ir ziņots par dažādu fukoidānu farmakoloģisku iedarbību, tostarp antioksidantu, pretaptaukošanās, pretdiabēta, pretnovecošanās, pretmikrobu, pretvēža (modulējot saimniekorganisma imūnsistēmu un kavējot audzēja angioģenēzi), antikoagulantu un pretiekaisuma iedarbību.1
Fucus vesiculosus samazina transsialidāzes aktivitāti asinīs, enzīmu, kas saistīts ar holesterīna uzkrāšanos pat par 36 %.3 Tas var būt noderīgi pacientiem ar zemu vairogdziedzera darbību, jo lēna vielmaiņa ir saistīta ar pārmērīgu lipīdu un glikozes uzkrāšanos.
Apkopojot Fucus vesiculosus labās īpašības, jāmin, kā tās efektīvi attīra organismu no šlakām un toksīniem, uztur endokrīnās sistēmas veselību. Iesaka lietot pie hipotireozes, asinsrites traucējumiem, saindēšanās ar smago metālu sāļiem. Fucus vesiculosus palēnina aterosklerozes attīstību, samazina holesterīna līmeni asinīs. Brūnaļģes polisaharīdi piebriest, palielina savu apjomu un kairina zarnu gļotādas, līdz ar to stimulē peristaltiku, veicina zarnu attīrīšanu, kas tiek izmantots svara mazināšanai cilvēkiem ar aptaukošanos. Polisaharīdi saista toksīnus, izvada tos no organisma. Brūnaļģes algināti izvada no organisma smagos metālus un radionukleīdus. Brūnaļģes satur vairāk mikroelementu nekā sauszemes augi.
Fucus vesiculosus drošību pamatojošu klīnisku pētījumu nav, taču, pamatojoties uz Fucus kā tradicionāla ēdiena lietošanu, mērens jūras aļģu patēriņš parasti tiek uzskatīts par drošu. Jūraszāles var tiktpakļautas ķīmiskajam piesārņojumam, kas atrodas ūdenī, kurā tās ir ievāktas, tāpēc ir īpaši svarīga to izcelsme un ražotāja kvalitātes prasības. Ir ziņots par Fucus nefrotoksicitātes gadījumiem, iespējams, arsēna piesārņojuma dēļ. Tādēļ pievērsiet uzmanību, ja aļģu saturoši produkti ir neparasti lēti vai tie nav reģistrēti pārtikas drošības institūcijās.
Ierobežoto pētījumu dēļ, nav precīzi definētu ieteikumu brūnaļģudienas devām, tomēr lielākoties iesaka nepārsniegt 500 mg dienas devu.
Grūtniecība un zīdīšanas periods: Fucus vesiculosus, iespējams, nav droši lietot grūtniecības vai zīdīšanas laikā, ja vien to nav nozīmējis ārsts.
Alerģija pret jodu: Fucus vesiculosus var saturēt lielu daudzumu joda, kas jutīgiem cilvēkiem var izraisīt alerģisku reakciju. Neizmantojiet tās kā pārtikas produktu pārmērīgā daudzumā, taču kā uztura bagātinātāju ar kontrolētu vielu daudzumu drīkst izmantot.
Ķirurģija: Fucus vesiculosus var palēnināt asins recēšanu. Tas var izraisīt papildu asiņošanu operācijas laikā un pēc tās. Pastāstiet savam ārstam, kādā apjomā lietojiet aļģes un nepieciešamības gadījumā pārtrauciet lietot Fucus vesiculosus vismaz 2 nedēļas pirms operācijas, ja ārsts tā ir norādījis.
Mijiedarbība ar medikamentiem:
Esiet piesardzīgi, ja lietojat:
Fucus vesiculosus lietošana kopā ar litiju var palielināt vairogdziedzera funkcijas izmaiņu risku.
Fucus vesiculosus lietošana kopā ar zālēm hiperaktīvam vairogdziedzerim var mainīt šo zāļu iedarbību.
Fucus vesiculosus var palēnināt asins recēšanu. To lietošana kopā ar zālēm, kas arī palēnina asins recēšanu, var palielināt zilumu un asiņošanas risku.1
Mūsu platuma grādos bieži sastopama parādība ir vairogdziedzera samazināta funkcija jeb hipotireoze. Tāda ir gandrīz katrai trešajaivai ceturtajai sievietei. Sievietes šī problēma skar vairāk, jo vairogdziedzera funkciju un tā darbību iespaido psihoemocionālais stāvoklis. Vairogdziedzeris ļoti jutīgi reaģē uz adrenalīnu un stresa hormonu kortizolu. Tipiskas hipotireozes pazīmes ir salīgums, šķidruma aizture un jo īpaši tas izpaužas pirmsmenopauzes vecumā.1
Vesela pieauguša cilvēka ķermenis satur 15 līdz 20 mg joda, no kuriem 70 līdz 80 % atrodas vairogdziedzerī. Hroniska joda deficīta gadījumā, joda saturs vairogdziedzerī var nokrist zem 20 µg. Ja organismam ir pieejams pietiekošs joda daudzums, tadvairogdziedzeris “izlieto” aptuveni 60 µg joda dienā, lai līdzsvarotu tā zudumu un uzturētu vairogdziedzera hormonu sintēzi, attiecīgi jods ir būtiska vairogdziedzera ražoto hormonu sastāvdaļa.2
Organisms neražo jodu, tāpēc ir būtiski lietot pārtikas produktus, kas satur jodu vai arī uzņemt jodu ar pārtikas piedevām vai uztura bagātinātājiem. Jods ir atrodams dažādos pārtikas produktos, tomēr jūras produktiem ir augstāks joda saturs, jo jūras augi un dzīvnieki spēj koncentrēt jodu no jūras ūdens. Lielos daudzumos jods organiskā veidā sastopams aļģēs, t.sk. Fucus vesiculosus. Jaorganismā nav pietiekami daudz joda, tas nevar ražot pietiekamādaudzumā vairogdziedzera hormonus. Tādējādi joda deficīts var izraisīt vairogdziedzera palielināšanos, hipotireozi un intelektuālās attīstības traucējumus zīdaiņiem un bērniem, kuru mātēm grūtniecības laikā ir bijis joda deficīts.3 Riskam īpaši ir pakļauti striktie vegāni, jo viņu ikdienas pārtikas produkti ir ierobežoti.4
Fucus vesiculosus satur flavonoīdu fukoksantīnu un tiek ziņots, ka tam ir visaugstākā antioksīdatīvā darbība ēdamo jūraszāļu vidū.Fucus vesiculosus, kurās ir daudz minerālvielu un halogenīdi, tostarp jods, ir izrādījis labvēlīgu ietekmi vairogdziedzera disfunkcijas ārstēšanā, piemēram, Hašimoto slimība un subklīniski
hipotireoze. Fucus ir arī spēja samazināt transsialidāzes aktivitāti asinīs, kas ir saistīta ar holesterīna uzkrāšanos. Tas var būt svarīgi pacientiem ar samazinātu vairogdziedzera funkciju, kuru vielmaiņa ir saistīta ar hiperlipidēmiju.5

Lavanda (Lavandula angustifolia L.)
Lavandu dabiskais izplatības areāls galvenokārt ir Kanāriju salas, Āfrikas ziemeļi un austrumi, Austrālija, Dienvideiropa, Arābijas pussala un Indija. Lavandas ziedus izmanto aromterapijā, jo tiem piemīt nomierinoša iedarbība uz centrālo nervu sistēmu, kā arī uz elpceļu nervu sistēmu. Tāpat lavandu ļoti plaši izmanto medicīniskiem nolūkiem, piemēram, lietojot iekšķīgi lavandas eļļu saturošas kapsulas, tā veicina ikdienas mierīgumu, noturību pret stresu, aizmigšanu un labu miegu.
Lavanda ir daudzgadīgs lūpziežu jeb panātru dzimtas augs ar tūkstošiem gadu ilgu vēsturi. Mazs, smaržīgs krūms, kura maksimālais augstums ir 80 centimetri un tas ir gan nektāraugs, gan ēteriskās eļļas augs. Lavandām ir pretēji sakārtotas, pelēkzaļas, lancetiskas lapas ar ieritinātu malu. Ziedi divlūpaini, zili vai violetzili, sakopoti neīstos mieturos, kas savukārt veido skraju vārpu ziedneša galā.
Lavandas ģints ietver līdz pat 47 sugām. Dabiskos apstākļos lavandas aug ziemeļu un austrumu Āfrikā, Austrālijā, Arābijas pussalā, Indijā, Kanāriju salās un Dienvideiropā. Tomēr kākultūraugs sastopams visā pasaulē.
Nraugoties uz lielo sugu daudzveidību, izšķirami trīs galvenie veidi: angļu, spāņu un franču lavanda. Lai arī tām ir daudz līdzību, franču un angļu šķirnes var atšķirt pēc izskata, augšanas paradumiem, ziedēšanas laika, aromāta un pielietojuma.
Angļu vai “īstā” lavanda (Lavandula officinalis angustifolia) irdruknāka, ar pilnīgāku ziedu un tieši šo lavandas sugu lielākoties izmanto medicīniskiem nolūkiem.
Tās ziedi satur 3% ēterisko vielu, antocianīnus, fitosterīnus, cukurus, minerālvielas un tanīnus. Lavandas ēteriskās eļļas kvalitatīvais un kvantitatīvais sastāvs ir mainīgs un atkarīgs no genotipa, augšanas vietas, klimatiskajiem apstākļiem, pavairošanas un morfoloģiskajām iezīmēm. Lavandas ēteriskajā eļļā ir vairāk kā 300 dažādas ķīmiskaskompozīcijas, no kurām galvenās ir linalols (daudzums variē no 9.3% līdz 68.8% un tam piemīt šādas ārstnieciskās īpašības: pretiekaisuma, pretkrampju, relaksants, pretsāpju līdzeklis, nomierinošs līdzeklis, antidepresants, pretstresa līdzeklis un anksiolītisks līdzeklis), linalilacetāts (daudzums variē no 1.2% līdz59.4%), lavandulyl acetāts, ocimēns, cineols un terpinen-4-ols. Lavandas ēteriskajai eļļai piemīt labas antioksidanta un pretmikrobu aktivitātes, ja to lieto uz ādas, kā arī būtiska pozitīva ietekme uz gremošanas un nervu sistēmu lietojot iekšķīgi.
Linalols un linalilacetāts tiek uzskatīti par lavandas eļļas galvenajām sastāvdaļām, kas varētu būt saistītas ar miegu veicinošo iedarbību, modulējot glutamāta un GABA iedarbību.
Ir pierādīts, ka lavanda darbojas kā anksiolītisks (trauksmes mazināšanas) līdzeklis un kā nomierinošs līdzeklis, lai palielinātuorganisma relaksāciju un atslābumu, tādējādi veicinot aizmigšanu.
Lavanda mijiedarbojas ar neiromediatoru (ķīmiska viela, kas dabiski veidojas nervu sistēmā, ļaujot nervu šūnām savstarpēji sazināties un to trūkums vai pārmērīgs daudzums var izraisīt dažādus garastāvokļa traucējumus) GABA, lai palīdzētu nomierināt smadzeņu un nervu sistēmas darbību, mazinot uzbudinājumu, dusmas, agresiju un nemieru. Lavanda arī darbojas kā pretsāpju līdzeklis.
Lavandas eļļas toksicitāte nerada bažas. Tādi komponenti kā linalols un linalilacetāts nav mutagēni. Ņemot vēra, ka lavandu lieto arī pārtikā, tā ir droša arī tad, ja to lieto kā medikamentus. Blakusparādības var būt aizcietējumi, caureja un galvassāpes.
Esiet piesardzīgi lietojot sedatīvos medikamentus (centrālo nervu sistēmu nomācošus līdzekļus) kopā ar lavandu, jo tie savstarpēji mijiedarbojas.
Lavanda var izraisīt miegainību un palēninātu elpošanu. Arīsedatīvie līdzekļi (zāles), var izraisīt miegainību un palēninātu elpošanu. Lavandas lietošana kopā ar sedatīviem medikamentiem var izraisīt elpošanas problēmas un/vai pārmērīgu miegainību.
Bezmiegs ir viens no visizplatītākajiem miega traucējumiemiedzīvotāju vidū. Šis traucējums ir arī starp biežākajām sūdzībām primārās veselības aprūpes centros. Lavandu dažādās austrumu tradicionālajās medicīnās sauc par "smadzeņu slotu", jo tā spēj “iztīrīt” galvu līdzīgi kā slota izslauka istabu no gružiem. Tas ir viens no visbiežāk lietotajiem augiem pacientiem ar miega traucējumiem.
Saskaņā ar Eiropas Zāļu aģentūras novērtējuma ziņojumuEMA/HMPC/143183/2010, lavandas eļļa darbojas kā nomierinošs līdzeklis un veicina miegu. Atsevišķi pētījumi ir pierādījuši, ka personas nākamajā rītā pēc lavandas iedarbības ziņoja par lielāku mundrumu un sparu, kā arī lavandas iedarbībā palielinājās non-REM jeb lēnā miega vieglās fāzes stadija un samazinājās nemierīgā miega fāze jeb ātrais miegs (REM - ātrās acu kustības) un tā ilgums.
Vienlaikus paildzinājās pamošanās laiks pēc pirmās aizmigšanas (pamošanās pēc miega sākuma).
Augi un augu izcelsmes zāles dažādu miega traucējumu ārstēšanaiizmantotas ārstnieciskos nolūkos jau gadsimtiem ilgi – arī lavanda.Dažādi, kompleksi bioķīmiski procesi smadzenēs nodrošina mums miegu, t.sk. mijiedarbība ar GABAerģiskajiem signāliem.
Kā galvenais inhibējošais neirotransmiters GABA palīdz uzturēt vispārējo līdzsvaru neironu ierosmes un inhibīcijas centrālajā nervu sistēmā un spēlē vienu no galvenajām lomām smadzeņu attīstībā un darbībā. Tiek uzskatīts, ka vairāk kā 20% no visiem smadzeņu neironiem ir GABAerģiski. Trīs dažādi GABA receptori: GABAA, GABAB un GABAC ir iesaistīti miega un uzbudinājuma regulēšanā (tiesa dažādos apmēros). Visbiežāk lietotās miega zāles iedarbojas tieši uz GABA sistēmām, jo īpaši benzodiazepīna.
Lavandas aktīvās sastāvdaļas var sasaistīt glutamāta N-metil-D-aspartāta receptorus (NMDA) un serotonīna transportētājus. Tiek uzskatīts, ka NMDA receptors ir ļoti svarīgs sinaptiskā plastiskuma kontrolei un un kalpo kā starpnieks atmiņas funkcijai. Miega veicinošie GABAerģiskie neironi ir bezmiega farmakoloģiskās terapijas galvenais mērķis.
Jāsaka gan, ka, neskatoties uz vairāku miega zāļu pieejamību, blakusparādības joprojām ir problēma, un joprojām ir pieprasījums pēc drošākām bezmiega ārstēšanas iespējām. Pētījumi liecina, ka vairākas augu izcelsmes vielas t.sk. lavandā sastopamās, var kalpot kā miegu veicinošas, modulējot GABAerģisko signālu pārraidi smadzenēs. Augu izcelsmes produktu drošums un plašā pieņemšana(blakusparādību neesamība) pacientu vidū ir spēcīgs arguments dotpriekšroku augiem, nevis rūpnieciski ražotām zālēm.

L-triptofāns (L-Tryptophan)
L-triptofāns ir neaizstājamā aminoskābe, dabisko olbaltumvielu sastāvdaļa. Augi un mikroorganismi triptofānu spēj sintezēt no indola un serīna. L-triptofāns ir svarīgs daudziem ķermeņa orgāniem. L-triptofānu organisms neražo, tāpēc tā uzņemšanai ir jāpievērš uzmanība. Pēc L-triptofāna absorbcijas no pārtikas,organisms daļu no tā pārvērš par 5-HTP (vielmaiņas starpprodukts neirotransmitera serotonīna biosintēzē) un pēc tam par serotonīnu.
Hopkinss un Kols atklāja triptofānu 1900. gadu sākumā pēc tam, kad to izdalīja no kazeīna proteīna, savukārt, Ellingers un Flamandspēc neilga laika noteica tā molekulāro struktūru. L-triptofāns (t.i., triptofāns) ir viena no astoņām neaizvietojamām aminoskābēm (aminoskābēm, kuras cilvēka organismā nevar sintezēt un kuras ir jāsaņem ar uzturu). Tātad L-triptofāns ir unikāla proteīna aminoskābe, kurai ir indola gredzens. Indols ir tipisks slāpekļa heterocikliskais aromātiskais savienojums, kas plaši izplatīts mūsu ikdienas produktos un dabiskajā vidē. Indola gredzens atrodas daudzos alkaloīdos, fitohormonos, augu ziedu eļļās, pigmentos un olbaltumvielās. Tā kā indola kodolam ir plašs bioloģisko aktivitāšu spektrs, to plaši izmanto farmācijas rūpniecībā.
Pēc L-triptofāna iekļūšanas dažādos organisma audos un šūnās, tastiek iekļauts olbaltumvielu metabolismā un sintēzē, kā arī tas varpiedalīties dažādos vielmaiņas procesos atkarībā no specifisku enzīmu aktivitāšu izpausme audos.
L-triptofāns ir vienīgais perifēri un centrāli ražotā serotonīna prekursors. Serotonīns regulē nervu sistēmas līdzsvaru, psihisko stabilitāti, garastāvokli un arī miegu. Savukārt, no serotonīna sintezējas melatonīns. Kā melatonīna "izejas materiāls" serotonīns palīdz regulēt miega ciklus un iekšējo pulksteni. Ir pierādīts, ka tieši melatonīnam ir noteicoša loma miega kvalitātē. Melatonīns ir bioloģiski aktīva viela, kas veidojas mūsu smadzenēs nakts laikā (tumsā) un regulē mūsu organisma bioritmus – miega un nomoda ciklu. Gan melatonīns, gan arī serotonīns veidojas no neaizvietojamās aminoskābes L-triptofāna, kuru mēs varam uzņemt tikai ar uztura vai uztura bagātinātāju palīdzību. Ievērojams L-triptofāna daudzums atrodams dažādos sieru veidos un gaļā.
L-triptofānu saturoši uztura bagātinātāji ir droši, ja tos nelieto ilgstoši. L-triptofāns var izraisīt dažas blakusparādības, piemēram, miegainību, sāpes vēderā, vemšanu, caureju, galvassāpes, neskaidru redzi, reiboni, sirdsklauves un kā arī citas.
L-triptofāns var traucēt daudzu dažādu zāļu darbību. Nelietojiet L-triptofānu, ja lietojat antidepresantus, kas pazīstami kā selektīvie serotonīna atgriezeniskās saistes inhibitori (SSAI), MAO inhibitori, tricikliskie antidepresanti un netipiski antidepresanti. Tas var izraisīt dzīvībai bīstamu stāvokli, ko sauc par serotonīna sindromu. Serotonīna sindroma simptomi ir:
- • Ārkārtīga trauksme
- • Sirdsklauves
- • Delīrijs
- • Smagas muskuļu spazmas
- • Paaugstināta ķermeņa temperatūra
L-triptofāna piedevas nav ieteicamas grūtniecēm.
Pirms L-triptofāna lietošanas konsultējieties ar savu ārstu, ja Jums ir aknu ciroze.
Vienmēr pastāstiet savam ārstam par jebkādiem uztura bagātinātājiem, ko lietojat, ieskaitot dabiskos un bez receptes iegādātos uztura bagātinātājus. Tādā veidā ārsts var pārbaudīt iespējamās blakusparādības vai mijiedarbību ar jebkādām zālēm.
L-triptofāna galvenā loma cilvēka organismā ir daļa no proteīnu sintēzes. Tā kā triptofāns no visām organismā esošajām aminoskābēm ir atrodams viszemākajā koncentrācijā, tas ir salīdzinoši mazāk pieejams un tiek uzskatīts, ka tam ir proteīnu sintēzes ātrumu ierobežojoša loma. Triptofāns ir arī divu svarīgu vielmaiņas procesu: kinurenīna sintēzes un serotonīna sintēzes perkusors (viela, kas iesaistīta reakcijā, kuras rezultātā veidojas mērķa viela - vielmaiņas ceļa starpposma dalībnieks).
Attiecīgi, serotonīns tiek sintezēts no cilvēka organismā neaizvietojamās aminoskābes - L-triptofāna, savukārt, serotonīns regulē noskaņojumu, uzlabo miega kvalitāti un ēstgribu. Būtiski, ka serotonīns piedalās arī dopamīna regulācijā - ja tas trūkst veicina tā izdalīšanos, ja dopamīns ir par daudz - palīdz piebremzēt tā izdalīšanos. Tiek uzskatīts, ka zems serotonīna līmenis ir cieši saistīts ar depresiju, trauksmi, miega traucējumiem, svara pieaugumu un citām veselības problēmām. Ja organismā ir serotonīna deficīts, tad cilvēkam pasliktinās garastāvoklis, pieaug pesimistisks un apātisks noskaņojums, kā rezultātā zūd vēlme kaut ko darīt.
Vairākas laboratorijas ir pierādījušas L-triptofāna pozitīvo efektu uz miega kvalitāti, kā arī to, ka triptofāns samazina laiku, kas nepieciešams, lai tie pacienti, kuriem ir viegls bezmiegs vai ilgs aizmigšanas laiks, aizmigtu.
Lietojot triptofānu, nav konstatēta nekāda ietekme uz modrību nākamajā dienā. Pacientiem ar vidēji smagu vai smagu bezmiegu triptofāns nav tik efektīvs kā standarta miega līdzekļi.
Kopumā varam teikt, ka serotonīns regulē nervu sistēmas līdzsvaru, psihisko stabilitāti, garastāvokli un arī miegu, ir “izejas materiāls” melatonīnam. Savukārt ir pierādīts, ka tieši melatonīnam ir noteicoša loma miega kvalitātē. Gan melatonīns, gan arī serotonīns veidojas no neaizvietojamās aminoskābes L-triptofāna, kuru mēs varam uzņemt tikai ar uztura vai uztura bagātinātāju palīdzību.
Tomēr, kad triptofāns tiek uzņemts kā daļa no uztura, tam pievienojas citas lielas neitrālas aminoskābes, kas sacenšas par sistēmu, kas tās visas transportē smadzenēs. Tā rezultātā triptofāna uzņemšana ar uzturu, atšķirībā no triptofāna uztura bagātinātājuveidā, nepaaugstina triptofāna līmeni smadzenēs. Tādējādi populārais mīts, ka piena glāzei pirms gulētiešanas ir nomierinošaiedarbība, jo tajā ir triptofāns, ir maldīgs.

D vitamīns
D vitamīns ir prohormons (hormonu prekursors) taukos šķīstošo vitamīnu grupā. Ir pieci D vitamīna veidi — sākot no D1 līdz D5, kur izplatītākās ir divas formas: D3 vitamīns jeb holekalciferols un D2 vitamīns jeb ergokalciferols.
D vitamīns palīdz regulēt kalcija un fosfāta daudzumu organismā un tas ir nepieciešamas, lai saglabātu kaulu, zobu un muskuļu veselību. Pētījumos ir secināts, ka D vitamīna deficīts ir saistāms ar depresiju un neirokognitīvo disfunkciju, vairākiem ļaundabīgiem audzējiem un vispārēju mirstības palielināšanos. Jauni pētījumi pierāda būtisku D vitamīna lomu optimāla miega uzturēšanā un regulēšanā, kā arī savstarpējo saistību starp D vitamīna koncentrāciju, miega ilgumu un kaulu vielmaiņu. D vitamīns var modulēt iedzimto un adaptīvo imūnreakciju. Savukārt šī vitamīna deficīts ir saistīts ar paaugstinātu autoimunitāti, kā arī paaugstinātu uzņēmību pret infekcijām.
D vitamīns ir prohormons, kas pieder taukos šķīstošo vitamīnu grupai; tas tiek sintezēts organismā, kad saules ultravioletais B (UVB) starojums mijiedarbojas ar prekursoru molekulu, 7-dehidroholesterīnu (7-DHC), ādā (lai gan tiek lēsts, ka veseliem cilvēkiem iekšēja D vitamīna ražošana veido 90% no kopējā daudzuma, neliels D vitamīna daudzums tiek saņemts arī no uztura un papildus piedevām). Pēc tam D vitamīns tiek transportēts asinīs (saistīts ar D vitamīnu saistošo proteīnu) uz aknām, kur tas tiek hidroksilēts līdz 25-hidroksivitamīnam D (25-(OH)D). 25-(OH)D tālāk pārvēršas metaboliski aktīvajā formā 1α, 25-dihidroksivitamīns D (1α, 25-(OH)2D), galvenokārt nierēs. D vitamīns regulē kalcija jonu un fosfātu daudzumu un uzsūkšanos tievajā zarnā, nodrošina kaulu un zobu veidošanos, kā arī palīdz nostiprināt imūnsistēmu.
Tātad, lai vitamīns D aktivizētos, nepieciešamas divas metabolas pārvērtības – vispirms aknās – hidrolizācija 25. pozīcijā (25(OH)D) un tad nierēs – 1-α- hidrolizācija, pēc kuras aktīvais vitamīns D spēj saistīties ar vitamīna D receptoriem, lai piedalītos gēnu transkripcijā un regulētu jonu (Ca/P) homeostāzi.
Ja apskatām D vitamīna izplatītākās formas D2 (ergokalciferols vai kalciferols) un D3 (holekalciferols), tad ir zināms, ka ergokalciferolu galvenokārt iegūst no augu izcelsmes avotiem, ko veido UVB starojumsaugu un sēņu šūnu membrānās.
Turklāt D2 vitamīns ir sintētiska molekula, ko lieto pārtikas produktu uzlabošanai - pievieno maizei, graudaugiem un piena produktiem, kā arī lieto uztura bagātinātājos. Savukārt D3 vitamīns tiek iegūts no “dzīviem” avotiem, piemēram, zivju eļļas, dzīvnieku aknām un olas dzeltenumiem. Tieši D3 vitamīns veidojas arī ādā no provitamīna D3 (7-DHC).
D vitamīna deficīts tiek uzskatīts par miega riska faktoru, jo pētījumos ir novērota D vitamīna un miega ilguma korelācija. Miega pētījumi ir parādījuši, ka zemāks D vitamīna līmenis ir saistīts ar īsu miega ilgumu visa vecuma cilvēkiem.
D vitamīna būtiska funkcija ir aktivēt T leikocītus – šūnas, kas faktiski atklāj un iznīcina svešus mikroorganismus, piemēram, vīrusus. Tādēļ uz visu balto asins šūnu (leikocītu) virsmām atrodas D vitamīna receptori. D vitamīns var modulēt iedzimtās un adaptīvās imūnās atbildes. Tā deficīts ir saistīts ar paaugstinātu autoimunitāti, kā arī paaugstinātu uzņēmību pret infekcijām. Tā kā imūnās šūnas autoimūno slimību gadījumā reaģē uz D vitamīnu pozitīvi, tam ir labvēlīga ietekme šo slimību kontrolē.
D vitamīna deficīts var rasties dažādu iemeslu dēļ:
D vitamīna deficīts var izraisīt kaulu blīvuma samazināšanos, kas var veicināt osteoporozi un kaulu lūzumus. Ir novērots, ka personām ar D vitamīna trūkumu ir “caurs” un nenoturīgs miegs, kā arī citi miega traucējumi.
Smags D vitamīna trūkums var izraisīt arī citas slimības. Bērniem tas var izraisīt rahītu. Rahīts ir reta slimība, kuras rezultātā kauli kļūst mīksti un liecas. Pieaugušajiem smags D vitamīna deficīts izraisa osteomalāciju. Osteomalācija izraisa vājus kaulus, kaulu sāpes un muskuļu vājumu.
Pētnieki pēta D vitamīnu, lai noskaidrotu tā iespējamo saistību ar vairākiem veselības traucējumiem, tostarp diabētu, augstu asinsspiedienu, vēzi un autoimūnām slimībām, piemēram, multiplo sklerozi.
Ir daži pārtikas produkti, kas dabiski satur D vitamīnu: treknas zivis(piemēram, lasis, tuncis un skumbrija), liellopu aknas, siers, sēnes un olu dzeltenumi.
D vitamīnu var iegūt arī no bagātinātiem pārtikas produktiem. Varat pārbaudīt pārtikas produktu etiķetes, lai uzzinātu, vai pārtikā ir D vitamīns. Pārtikas produkti, kuriem bieži tiek pievienots D vitamīns, ir:piens, brokastu pārslas un apelsīnu sula.
Pieaugušiem cilvēkiem bez D vitamīna deficīta ieteicamā D vitamīna dienas deva ir 15 mcg jeb 600 IU, pēc 70 gadu vecuma: 20 mcg jeb 800 IU.
Pārmērīgs D vitamīna daudzums ir toksisks. Tā kā D vitamīns palielina kalcija uzsūkšanos kuņģa-zarnu traktā, D vitamīna toksicitāte izraisa izteiktu hiperkalciēmiju, hiperkalciūriju un augstu seruma 25(OH) līmeni. Hiperkalciēmija savukārt var izraisīt sliktu dūšu, vemšanu, muskuļu vājumu, neiropsihiskus traucējumus, sāpes, apetītes zudumu, dehidratāciju, poliūriju, pārmērīgas slāpes un nierakmeņus.
Ārkārtējos gadījumos D vitamīna toksicitāte izraisa nieru mazspēju, mīksto audu pārkaļķošanos visā ķermenī (tostarp koronārajos asinsvados un sirds vārstuļos), sirds aritmijas un pat nāvi.
D vitamīna papildus lietošana var mijiedarboties ar vairāku veidu medikamentiem. Personām, kas regulāri lieto šīs un citas zāles, būtu ieteicams apspriest ar savu veselības aprūpes speciālistu D vitamīna lietošanu un devas.
Orlistat
Svara zaudēšanas līdzeklis Orlistat (Xenical® un alli®) kopā ar diētu ar samazinātu tauku saturu var samazināt D vitamīna uzsūkšanos no pārtikas un uztura bagātinātājiem, tādējādi samazinot 25(OH)D līmeni.
Statīni
Statīnu zāles samazina holesterīna sintēzi. Tā kā endogēnais D vitamīns ir iegūts no holesterīna, statīni arī var samazināt D vitamīna sintēzi. Turklāt liela D vitamīna uzņemšana, īpaši no uztura bagātinātājiem, var samazināt atorvastatīna (Lipitor®), lovastatīna (Altoprev® un Mevacor®) un simvastatīna (FloLipid™ un Zocor®) iedarbību, jo šie statīni un D vitamīns savstarpēji konkurē par vienu un to pašu metabolizējošo enzīmu.
Steroīdi
Lai mazinātu iekaisumu, bieži tiek izrakstīti kortikosteroīdu medikamenti: budesonīds, prednizolons, prednizons, deksametazons, hidrokortizons un metilprednizolons (piemēram, Deltasone®, Rayos® un Sterapred®). Šīs zāles var samazināt kalcija uzsūkšanos un traucēt D vitamīna metabolismu.
Tiazīdu grupas diurētiskie līdzekļi
Tiazīdu grupas diurētiskie līdzekļi (piemēram, Hygroton®, Lozol® un Microzide®) samazina kalcija izdalīšanos ar urīnu. Šo diurētisko līdzekļu kombinācija ar D vitamīna piedevām (kas palielina kalcija uzsūkšanos zarnās) var izraisīt hiperkalciēmiju, īpaši gados vecākiem cilvēkiem un personām ar novājinātu nieru darbību vai hiperparatireozi.
D vitamīns ir prohormons, kas pieder pie taukos šķīstošo vitamīnu grupas. Lai gan tradicionāli ir pierādīts, ka D vitamīns ir iesaistīts kalcija homeostāzē un kaulu veselībā, jaunākie pētījumi ir atklājuši pozitīvu saistību starp D vitamīnu un miegu. Jo īpaši, klīniskie pētījumi ar cilvēkiem, liecina, ka zems D vitamīna līmenis ir saistīts ar sliktu miegakvalitāti un īsu miega ilgumu. D vitamīna receptori ir atrasti smadzeņu reģionos, kas iesaistīti miega regulēšanā, un šķiet, ka D vitamīns ir iesaistīts miega un nomoda cikla regulēšanā.
Kā mēs zinām, D vitamīnam ir nozīmīga loma kaulu homeostāzē un zems šī vitamīna līmenis ievērojami korelē ar zemu kaulu minerālo blīvumu (KMB). Miegs ir svarīgs kaulu vielmaiņas faktors un pētījumi ir atklājuši saistību starp miega ilgumu un KMB. Vairākos
pašnovērtējumu pētījumos ir ziņots, ka miega ilguma samazināšanās ir saistīta ar KMB samazināšanos un kortikālā kaula biezumu.
Saskaņā ar pētījumiem, miega ilgums mazāk nekā 5 - 6 stundas ir saistīts ar zemāku KMB un lielāku osteoporozes risku pieaugušajiem. Bērniem īss miega ilgums (<8 h) var būt saistīts ar kaulu masas uzkrāšanās traucējumiem īpaši straujas augšanas periodos. Hronisks miega trūkums var tieši ietekmēt kaulu vielmaiņu. Šie atklājumi liecina, ka miega trūkums var būt riska faktors sliktākai skeleta veselībai kaulu vielmaiņastraucējumu dēļ, var pasliktināt kaulu mikroarhitektūru un samazināt KMB.
Rezumējot, pastāvīgs D vitamīna deficīts var ietekmēt miega ilgumu, savukārt nepilnvērtīgs miegs rada risku kaulu lūzumiem un osteoporozei dēļ traucētas kaulu vielmaiņas.
Tādu infekcijas slimību ārstēšanai kā tuberkuloze, D vitamīns neapzināti ir jau lietots pirms efektīvu antibiotiku parādīšanās. Tuberkulozes slimniekus nosūtīja uz sanatorijām, tā saucamajām “saules peldēm”, kur ārstēšana sevī ietvēra saules gaismas iedarbību, tādējādi nogalinot tuberkulozi. Arī mencu aknu eļļa, kas ir bagātīgs D vitamīna avots, ir izmantota tuberkulozes ārstēšanai, kā arī vispārējai pastiprinātai aizsardzībai pret infekcijām.
D vitamīna labvēlīgā ietekme uz organisma aizsardzību daļēji ir saistīta ar tā ietekmi uz iedzimto imūnsistēmu. Ir zināms, ka makrofāgi atpazīst lipopolisaharīdus (pazīstami kā endotoksīni, kas veidojas, ejot bojā baktērijām), izmantojot TLR receptorus, kas izraisa imūnšūnu reakciju. TLR iesaistīšanās izraisa notikumu kaskādi, kas ražo pretmikrobu peptīdus ar spēcīgu baktericīdu aktivitāti, kas izjauc baktēriju šūnu membrānas, piemēram, katelicidīnu un beta defensīnu.
Ar tiešu D vitamīna piedalīšanos, mūsu ķermenis ražo vairāk nekā 200 pretmikrobu peptīdus, no kuriem spēcīgākais ir tieši katelicidīns, dabiska plaša spektra antibiotika. Šis fakts izskaidro D vitamīna terapijas efektivitāti visu veidu akūtu elpceļu vīrusu infekciju ārstēšanā.
Kopumā D vitamīns palīdz samazināt vīrusu replikāciju, inducējot defensīnus un katelicidīnus, un minimizē kopējo citokīnu (bioķīmiski aktīvas imūnās sistēmas savstarpējās saziņas proteīnu molekulas, ko imūnās sistēmas šūnas ražo, lai iedarbotos uz citām imūnšūnām) daudzumu, kas traumē plaušu gļotādu ar iekaisumu izraisošu pneimoniju, kā arī palīdz paaugstināt pretiekaisuma citokīnus.

Kalifornijas magone (Eschscholzia californica L.)
Kalifornijas magoni medicīnā lieto miega traucējumu (bezmiega), sāpju, nervu uzbudinājuma, kā arī urīnpūšļa un aknu slimību gadījumos. Kalifornijas magone satur dažādus dabiskus savienojumus, tostarp vairākus alkaloīdus, kas atrodami tikai šajā augā. Nomierinošās, trauksmes mazinošāsun pretsāpju iedarbības dēļ šis augs tiek izmantots farmācijā daudzās valstīs. Kalifornijas magonē konstatētie alkaloīdi iedarbojas uz GABA (gamma aminosviestskābes) receptoriem, kuru galvenā loma ir samazināt neironu uzbudināmību visā nervu sistēmā.
Kalifornijas magones ir magoņu dzimtas (Papaveraceae) ešolciju ģints augi. Tās, atkarībā no augšanas vietas, iedala divās lielās apakšsugās E.californica subsp. californica un E.californica subsp. mexicana.
Kalifornijas magones dabīgais izplatības areāls ir ASV (štati: Kalifornija, Oregona, Vašingtona, Nevada, Arizona, Ņūmeksika) un Meksika (štati: Sonora un Baja California), taču tas kā košumaugs ir izplatīts visā pasaulē.
Kalifornijas magone ir viengadīgs (vietās, kur nav to dabīgais augšanas areāls) vai daudzgadīgs 130-152 cm garš augs. Ziedi ir no dzeltenas līdz oranžai krāsai. Zied no februāra līdz septembrim (dabīgajās izplatības vietās)un ziediem piemīt specifisks aromāts.
Kalifornijas magoņu lapas indiāņi esot izmantojuši kā ārstniecības līdzekli, bet putekšņus – kosmētikā. Sēklas, savukārt, var izmantot kulinārijā.
Kalifornijas magones ir pazīstamas ar to nomierinošo, trauksmi mazinošo un miegu veicinošo iedarbību. Šis efekts tiek saistīts ar protopīnu un alokriptopīnu. Abi alkaloīdi darbojas kā vāji stimulatori - GABA receptoru ierosinātāji (agonisti) un kā acetilholīnesterāzes inhibitori, kas novērš acetilholīna (ACh) sadalīšanos un palielina darbības ilgumu un ACh līmeni nervu galos, ko sauc par sinapsēm. Cits no šī auga izolēts aporfīna alkaloīds, proti, N-metillaurotetanīns (NMT), darbojas kā serotonīna 5HT1AR receptoru bloķētājs (antagonists). Ir konstatēts, ka protopīns un alokriptopīns bloķē cilvēka serotonīna un noradrenalīna transportētājus (hSERT un NERT) un tiem piemīt antidepresantiem līdzīga iedarbība.
Kalifornijas magonēs, bez minētiem alkaloīdiem, ir arī citi aktīvi komponenti: alkaloīdi - kriptopīns un helidonīns, kā arī flavonoīdi unglikozīdi.
Kalifornijas magonēm nav narkotiskas iedarbības un tās ir pilnīgi drošas lietošanā. Tas nav opiātu dzimtas augs. Ja opija magonēm ir dezorientējoša iedarbība, Kalifornijas magonēm ir normalizējoša iedarbība uz cilvēka fizioloģiju un psiholoģiju. Alkaloīdiem ir nomierinoša un relaksējoša iedarbība uz ķermeni un prātu, bet tie darbojas maigi.
Kalifornijas magones ir drošas lielākajai daļai cilvēku, ja tās pareizi lieto iekšķīgi līdz trīs mēnešiem. Nav pietiekami daudz pētījumu par Kalifornijas magones lietošanas drošību, lietojot tās ilgstoši.
Ja plānota kirurģiska iejaukšanās: Kalifornijas magones iedarbojas uz centrālo nervu sistēmu, izraisot miegainību un citas pazīmes. Pastāv iespējamība, ka Kalifornijas magones var pārāk palēnināt centrālo nervu sistēmu, ja to lieto kopā ar anestēziju un/vai citām zālēm, ko lieto operācijas laikā un pēc tās. Pārtrauciet lietot Kalifornijas magoņu preperātus vismaz 2 nedēļas pirms plānotās operācijas.
MIJIEDARBĪBA
Sedatīvie medikamenti (benzodiazepīni un CNS nomācoši līdzekļi )
Mijiedarbības novērtējums: Mērens. Esiet piesardzīgi, lietojot šo kombināciju. Runājiet ar savu veselības aprūpes speciālistu.
Kalifornijas magones var izraisīt miegainību. Kalifornijas magoņu lietošana kopā ar sedatīviem medikamentiem var izraisīt pārāk lielu miegainību.
Dažas no šīm nomierinošajām zālēm ir klonazepāms (Klonopīns), diazepāms (Valium), lorazepāms (Ativan), fenobarbitāls (Donnatal), zolpidēms (Ambien) un citi.
Kalifornijas magones nav ieteicams lietot:
Bezmiegs tiek definēts kā grūtības aizmigt vai uzturēt noturīgu miegu, ko izraisa dienas notikumu radītās sekas un nav saistīts ar vides apstākļiem vai nepietiekamu miega ilgumu. Starptautiskajā miega traucējumu klasifikācijā bezmiegs tiek uzskatīts par hronisku, ja tas saglabājas ilgstoši - vismaz trīs mēnešus ar biežumu vismaz trīs reizes nedēļā. Citos gadījumos bezmiegs tiekdefinēts kā īslaicīgs un to var uzskatīt par koriģējošu, akūtu vai ar trauksmi saistītu bezmiegu.
Augu izcelsmes zāļu komiteja (HMPC) un Eiropas zāļu aģentūra (EMA) ir secinājušas, ka Kalifornijas magoni var lietot vieglu garīga stresa simptomu mazināšanai un kā miega līdzekli.
Kalifornijas magoņu sedatīvās un anksiolītiskās īpašības ir pierādītasvairākos preklīniskos pētījumos. Lietojot šo augu, tika novērota miega laika pagarināšanās un samazināta kustību aktivitāte miega laikā.
Kalifornijas magones ķīmiskais sastāvs, tāpat kā visām citām magoņu dzimtas pārstāvēm, ir bagāts ar alkaloīdiem, jo īpaši protopīnu, berberīnu, alokriptopīnu, esholcīnu, kalifornidīnu. Augā ir atrasti flavonoīdi, jo īpaši rutoze. Kalifornijas magone satur dažādus karotinoīdus, piemēram, zeaksantīnu, kas nosaka auga krāsu.
Ārstnieciskās īpašības ir saistītas ar tās ķīmiskajā sastāvā esošiemalkaloīdiem. Pateicoties tieši alkaloīdiem, Kalifornijas magonei ir nomierinoša, spazmolītiska un pat pretsāpju iedarbība uz cilvēka ķermeni.
Ar Kalifornijas magones palīdzību var normalizēt miegu, atbrīvoties no bezmiega un alkaloīdu viegli spazmolītiskā un nomierinošā iedarbība ļauj izmantot auga ekstraktu psiholoģisku un fizisku problēmu un nervu traucējumu ārstēšanai.

Kalcijs
Kalcijs palīdz veidot kaulus un zobus un ir būtisks nervu, enzīmu, sirds, muskuļu un asins recēšanas funkcijām. Nepietiekama šī minerāla uzņemšana var izraisīt kaulu vājumu un palielināt lūzumu risku gados vecākiem cilvēkiem. Kalcijs ir dabisks miega līdzeklis, kas var palīdzēt aizmigt un nodrošināt mierīgu miegu, jo kalcijs palīdz smadzenēm izmantot aminoskābi triptofānu, lai ražotu miegu izraisošu dabīgu hormonu – melatonīnu, kas palīdz iemigt un uzturēt miegu.
Kalcijs ir minerāls, kas visbiežāk asociējas ar veseliem kauliem un zobiem, lai gan tam ir arī svarīga loma asins recēšanā, palīdzot muskuļiem sarauties. Vienlaikus kalcijs regulē normālu sirds ritmu un nodrošina nervu funkcijas, kā arī piedalās hormonu darbības regulācijā, mazina neiromuskulāro uzbudinājumu, piedalās B12 vitamīna uzsūkšanā un izmantošanā. Apmēram 99% no ķermenī sastopamā kalcija atrodas kaulos, bet atlikušais 1% atrodas asinīs, muskuļos un citos audos.
Asins plazmā kalcijs ir trīs veidos: 41% saistīts ar olbaltumiem un šādā veidā tas nevar šķērsot kapilāru membrānu; 9% kombinācijā ar anjoniem un starpaudu šķidrumu, spēj šķērsot kapilāru membrānu un 50% ir jonizēts un spēj šķērsot kapilāru membrānu. Kalcijam ir liela nozīme šūnu un ekstracelulārā (ārpus šūnu) šķidruma apmaiņā.Kalcija joni ir nepieciešami nervu impulsu pārvadē.
Neironos kalcijs ir galvenais elements un tas veic daudzus uzdevumus. Tas palīdz izplatīt elektriskos signālus pa aksoniem(nervu šūnu izaugumiem, kas novada nerva impulsus uz citām nervu šūnām). Tas iedarbina sinaptiskos savienojumus, lai nogādātuneirotransmiterus (pārnes nervu impulsu no sinapses uz šūnu)sinapsēs. Kalcijs ir iesaistīts arī atmiņas veidošanā, vielmaiņā un šūnu augšanā.
Visas šūnas no primitīviem vienšūnas organismiem līdz augsti diferencētiem neironiem smadzeņu garozā ir atkarīgas no kalcija metabolisma. Šis elements ir svarīgs dzīvos organismos, sevišķi šūnu fizioloģijā, kur Ca2+ kustība iekšā un ārā citoplazmā darbojas par signālu daudziem šūnu procesiem.
Uztura bagātinātājos kalcijs ir sastopams dāžādās formās, kur katrs no savienojumiem satur dažādu kalcija daudzumu jeb pamatvielu,elementāro kalciju. Uztura bagātinātājos visbiežāk tiek izmantotas šādas kalcija formas:
- • Kalcija karbonāts (40% elementārā kalcija)
- • Kalcija citrāts (21% elementārā kalcija)
- • Kalcija laktāts (13% elementārā kalcija)
- • Kalcija glikonāts (9% elementārā kalcija)
Kalcija karbonātā elementārā kalcija daudzums ir būtiski lielāks pār citiem savienojumiem, tomēr ir nepieciešams skābs ēdiens vai dzēriens, lai tas uzsūktos. Savukārt kalcija citrātā esošā skābe veicina savienojuma uzsūkšanos samazināta skābuma vidē un tas var būt efektīvāks cilvēkiem, kas lieto kuņģa skābi samazinošus preparātus.
Ilgstošs kalcija deficīts var izraisīt izmaiņas zobos (zobi pēkšņi var kļūt jutīgāki, mīkstāki un vieglāk ievainojami; var gadīties, ka uzkožot uz kāda cietāka ēdiena, zobs vienkārši pārlūst), kataraktu, izmaiņas smadzenēs un osteoporozi, kas izraisa kaulu trauslumu.
Kalcija deficīta pazīmes:
Personai ar kalcija deficītu var rasties:
- • muskuļu sāpes, krampji un spazmas,
- • sāpes augšstilbos un rokās, ejot vai kustoties,
- • nejutīgums un tirpšana rokās, kājās un pēdās, kā arī ap muti.
Šie simptomi var parādīties un izzust, taču tiem nav tendence izzust līdz ar aktivitāti. Ekstrēmākas sajūtas var liecināt par smagāku deficītu, kas var izraisīt: krampjus, aritmiju un pat nāvi.
Zems kalcija līmenis var izraisīt ārkārtēju nogurumu, kas ietver enerģijas trūkumu un vispārēju gausuma sajūtu. Tas var izraisīt arī bezmiegu. Nogurums, kas saistīts ar kalcija deficītu, var ietvert arī reiboni un dubultošanos, ko raksturo fokusa trūkums, aizmāršība un apjukums.
Ilgstošs kalcija deficīts var izraisīt:
- • sausu ādu
- • sausus, lauztus vai trauslus nagus
- • lūztošus matus
- • alopēciju, kas izraisa matu izkrišanu plankumu veidā
- • ekzēmu vai ādas iekaisumu, kas var izraisīt niezošus vai sausus plankumus
- • psoriāzi
Kauli labi uzglabā kalciju, taču, lai tie būtu spēcīgi, ir nepieciešams augsts kalcija līmenis. Ja kopējais kalcija līmenis ir zems, organisms var novirzīt daļu kalcija no kauliem uz organismam nepieciešamajiem procesiem, padarot tos trauslus un pakļautuslūzumiem.
Laika gaitā pārāk maz kalcija var izraisīt osteopēniju - minerālu blīvuma samazināšanos kaulos. Tas var izraisīt osteoporozi, kuras rezultātā kauli kļūst plānāki un neaizsargāti pret lūzumiem, kā arī sāpes un stājas problēmas.
Daži pētījumi liecina, ka kalcija deficīts var būt saistīts ar garastāvokļa traucējumiem, tostarp depresiju.
Ikvienam, kuram ir aizdomas, ka kalcija deficīts veicina depresijas simptomus, jākonsultējas ar ārstu. Pēc kalcija līmeņa pārbaudes ārsts var ieteikt uzņemt apildus kalciju.
Lai organisms varētu izmantot kalciju, ir vērts zināt dažas nianses:
- • kopā ar kalciju ir nepieciešams D vitamīns – abi palīdz viens otram pildīt savas funkcijas;
- • lai kalcijs stiprinātu kaulus un zobus, pietiekami jāuzņem fosfors;
- • nepieciešami attiecīgi fermenti kuņģa zarnu traktā, kas uzņemto kalciju izšķīdina;
- • pārmērīga kafijas, sāls lietošana veicina kalcija izdalīšanos no organisma;
- • kaulu aplaupītāji ir arī skābeņskābe, kas ir atsevišķu dārzeņu, piemēram, rabarberu un spinātu, sastāvā;
- • kakao un melnā tēja negatīvi iespaido kalcija uzsūkšanos organismā;
- • negatīvs efekts uz kalcija absorbciju ir lielam cukura, sāls, fosfātu un tauku daudzumam uzturā. Ātrās uzkodas, veikalos gatavi nopērkamie ēdieni, gaļas un desu izstrādājumi satur sevišķi lielu daudzumu fosfātu, tāpēc to patēriņam vēlams būt samērīgam;
- • uzsūkšanos kavē trekna un taukaina barība, baltmaize, kviešu klijas. Uzsūkšanos var veicināt C vitamīns un to saturošie produkti;
- • ikviena gastroenteroloģiska rakstura slimība mazina kalcija uzsūkšanās spēju.
Daži pārtikas produkti, kas ir bagāti ar kalciju: piena produkti, piemēram, piens, siers un jogurts; pupiņas; vīģes; brokoļi; tofu; sojas piens un spināti.
Pieaugušiem cilvēkiem, kuriem nav novērots kalcija deficīts, dienā būtu nepieciešami 1000 mg kalcija, personām pēc 51 gada vecuma – 1200 mg dienā.
Pastāv apgriezta sakarība starp kalcija uzņemšanu un uzsūkšanos. Kalcija uzsūkšanās no pārtikas ir aptuveni 45%, ja tiek uzņemti 200 mg dienā, bet tikai 15%, ja uzņemšana pārsniedz 2000 mg dienā. Vecums var ietekmēt arī ar uzturu uzņemto kalcija uzsūkšanos. Zīdaiņiem un maziem bērniem, kam nepieciešams ievērojams daudzums, lai izveidotu kaulus, kalcija uzsūkšanās ar uzturu ir pat 60%, bet pieaugušā vecumā tā samazinās līdz aptuveni 25% un turpina samazināties līdz ar vecumu.
Lietojot kalcija preperātus, var tikt novērota vēdera uzpūšanās, gāzes un aizcietējumi. Ļoti lielas kalcija devas var izraisīt nierakmeņus.
Mijiedarbība. Ja regulāri lietojat kādas recepšu vai bezrecepšu zāles, jautājiet savam ārstam, vai ir droši lietot papildus kalcija piedevas. Kalcijs var mijiedarboties ar zālēm sirds slimību, diabēta, epilepsijas un citu slimību ārstēšanai. Lielas D vitamīna devas var izraisīt bīstami augstu kalcija līmeni. Lielas kalcija devas var arī neļaut Jūsu ķermenim absorbēt minerālvielas, piemēram, dzelzi un cinku. Centieties lietot kalciju ar intervālu no vienas līdz divāmstundām pirms vai pēc citu uztura bagātinātāju vai medikamentu lietošanas. Ja gadījumā Jūs lietosiet kalciju vienlaikus ar citiem medikamentiem vai uztura bagātinātājiem, tie var savstarpēji saistīties ar šiem produktiem, un tie izdalīsies no jūsu ķermeņa neuzsūkušies.
Kalcija uztura bagātinātāji var mijiedarboties vai traucēt noteiktu zāļu lietošanu, un dažas zāles var pazemināt kalcija līmeni organismā. Šeit ir daži piemēri:
Riski. Ja Jums ir nieru slimības, sirds problēmas, sarkoidoze vai kaulu audzēji, nelietojiet kalcija piedevas, ja vien to neiesaka ārsts.
Pārdozēšana. Augsts kalcija līmenis asinīs var izraisīt sliktu dūšu, sausu muti, sāpes vēderā, neregulāru sirdsdarbību, apjukumu un pat nāvi.
Kalcijs ir tieši saistīts ar mūsu miega cikliem. Vienā pētījumā, kas publicēts “European Neurology Journal”, pētnieki atklāja, ka kalcija līmenis organismā ir augstāks dažos dziļākos miega līmeņos, piemēram, ātrās acu kustības (REM) fāzē. Pētījumā secināts, ka miega traucējumi, īpaši REM dziļā miega trūkums vai traucēts REM miegs, ir saistīti ar kalcija deficītu. Normāla miega gaita tika atjaunota pēc kalcija līmeņa normalizēšanās asinīs.
Kalcijs palīdz smadzenēm izmantot aminoskābi triptofānu, lai ražotu miegu izraisošu vielu melatonīnu.
Ja organismā trūkst kalcija, var tikt kavēti nervu impulsi un tie nebūs stabili, tādējādi radot pārmērīgu uztraukumu vai stresu. Turklāt nervu sistēma savā darbībā sastapsies ar daudziem šķēršļiem: tiks traucēta sirds saraušanās un izmainīsies muskuļu refleksu funkcija. Ja kalcija deficīts būs ilgstošs, būs novērojamsbezmiegs, grūtības aizmigt, slikts miegs un bieža pamošanās.
Kalcija deficīts var izraisīt citas saistītas slimības, piemēram, peptiskas čūlas, kas arī nopietni ietekmē miegu. Kalcija trūkums stimulē kuņģa skābes palielināšanos, ilgtoši paaugstināta skābe radīs kuņģa gļotādas bojājumus, pat čūlas. Šo procesu bieži pavada tādi simptomi kā grēmas, slikta dūša un nakts stress, kas radabezmiegu.
Vienlaikus jāmin, ka ir cieša saikne starp D vitamīna līmeni un kalcija līmeni, kur kalcija līmenis regulē lēnā miega fāzes veidošanos, savukārt, klasiskās D vitamīna funkcijas ietver kalcija transportu zarnās un kaulu mineralizēšanu, kas ir būtiski kalcija homeostāzei. Iespējams, ka miega traucējumi D vitamīna deficīta gadījumā var būt saistīti ar izmainītu kalcija līmeni. Zemāks kalcija līmenis serumā var būt saistīts ar vairāk traucētu miega un nomoda kontroli un atpūtas un aktivitātes ritmu.

Rauga (Saccharomyces cerevisiae) beta-glikāni
Β-glikāni ir glikozes polisaharīdi, kuri dabiski sastopami graudaugos, baktērijās, raugos, sēnēs un mikroaļģēs. Imūnsistēma ir tā attīstījusies, lai atpazītu β-glikānus un tos īpaši atpazīst šūnu receptori, tādējādi aktivizējot imūnās šūnas. Β-glikāni, atkarībā no to iegūšanas avota un veida, atšķiras pēc to primārās struktūras, molekulmasas, šķīdības, sazarojuma attiecības, saišu veidiem un fizioloģiskajiem efektiem, piemēram, hipoholesterinēmijas un imūnmodulācijas.
Β-glikāns ir ūdenī šķīstoša šķiedrviela, ko iegūst no auzām, miežiem, baktērijām, raugiem, aļģēm un sēnēm. Maizes rauga, tas ir, Saccharomyces cerevisiae, šūnu membrānās ir atrodams visvairāk β-glikānu. β-glikāns ir polisaharīds, kas sastāv no glikozes molekulām. Glikozes monomēri ir saistīti ar β-(1→3) glikozīdu saitēm baktērijās un aļģēs, savukārt glikozes monomēri ir saistīti ar β-(1→3) un β-(1→6) glikozīdu saitēm raugā un sēnēs. Auzās un miežos glikozes monomēri ir saistīti ar β-(1→4) un β-(1→3) glikozīdu saitēm. No baktērijām un aļģēm iegūtajam β-glikānam ir lineāra struktūra, savukārt β-glikānam, kas iegūts no rauga, sēnēm, auzām un miežiem, ir sazarota struktūra. Β-glikāna sintēze šūnu sieniņā ir sarežģīts process, jo tiek identificēts liels skaits dažādu glikānu klašu. B-glikāna sintēzē ir iesaistītas vairākas enzīmu klases. Nav būtiskas atšķirības starp nešķīstošo un šķīstošo β-glikāna frakcijām, tomēr β-glikāna šķīdība ūdenī ir atkarīga no tā struktūras.
Tātad sēnes, baktērijas un augi ražo dažādus glikānus ar lielām atšķirībām to 1→3, 1→4 un 1→6 β-glikozīdu saišu proporcijās un izkārtojumā, attiecīgi tie ir dažādi β-glikānu tipi jeb veidi. Šie trīs veidi atšķiras ne tikai molekulārā līmenī, bet arī atšķirīgi ietekmē ķermeni. Lai gan katrs no šiem β-glikānu veidiem var pozitīvi ietekmēt veselību, ieguvumi atšķiras atkarībā no β-glikāna veida.
No auzām iegūtie β-glikāni ir labi, lai veicinātu sirds veselību un palīdzētu kontrolēt ZBL (sliktā) holesterīna līmeni. Tie uzlabo vielmaiņas parametrus, piemēram, dislipidēmiju un insulīna rezistenci.
Lai gan ir pierādīts, ka no sēnēm iegūtiem β-glikāniem ir labvēlīga ietekme uz imūnsistēmu, pētījumi liecina, ka to iedarbība tomēr ir zemāka nekā dažiem labi izpētītiem maizes rauga β-glikāniem.
No rauga iegūtie β-glikāni darbojas kā imūnmodulatori, īpaši stimulējot iedzimto imūno atbildi. Tie parasti rodas maizes raugā vai alus raugā. Lai gan abi ir β-(1→3) un β-(1→6) glikāni no Saccharomyces cerevisiae, avots ir svarīgs — no maizes rauga šūnu membrānām ekstrahētajiem β-glikāniem ir atšķirīgs molekulārais modelis nekā alus rauga molekulārajai struktūrai, kas var ietekmēt imūnmodulējošās (imunitāti veidojošās) īpašības.
Aktivizējot un uzlabojot imūnās šūnas, β-glikāni palīdz organismam cīnīties pret vīrusiem, baktērijām un citiem patogēniem.
Tomēr ir būtiski izvēlēties augstas kvalitātes β-glikānus, jo tie nodrošina bioloģisko aktivitāti un vēlamo darbības mehānismu organismā. Β-glikānu ekstrahēšanai izmantotās ražošanas vai apstrādes metodes var ietekmēt to struktūru. Ja β-glikānu struktūra ir bojāta vai mainīta ražošanas procesa laikā, gatavajā produktā imunitāti stiprinošs rezultāts var nesekot.
Nav ziņu par beta glikānu deficītu. Turklāt beta glikāniem nav noteikta ieteicamā uztura deva (NRV). Tomēr, ņemot vērā, ka beta glikāni ir šķiedrviela, ir ieteikumi par vēlamo šķiedrvielu uzņemšanas daudzumu, un, diemžēl, daudzi cilvēki savā uzturā nelieto pietiekami daudz šķiedrvielu.
Būtu vēlams uzņemt vismaz 14 gramus šķiedrvielu uz 1000 uzņemtām kalorijām. Šķiedrvielu ieteicamais daudzums atšķiras sievietēm un vīriešiem, tā, piemēram, tas svārstās no 21 līdz 26 gramiem šķiedrvielu dienā sievietēm un no 30 līdz 38 gramiem dienā vīriešiem, atkarībā no vecuma.
Beta glikāni dabiski ir sastopami dažādos pārtikas produktos. Labi to avoti ir: auzas, mieži, sorgo, rudzi, kukurūza, kvieši, rīsi, sēnes, jūraszāles (aļģes).
Tādos graudaugos kā mieži un auzas ir visaugstākā beta glikānu koncentrācija. Turklāt šī šķiedrviela ir atrodama dažu veidu baktērijās un sēnēs, tostarp Saccharomyces cerevisiae, ko izmanto uztura rauga, vīna, alus un dažu maizes izstrādājumu pagatavošanai. Tomēr tas nenozīmē, ka alkoholiskie dzērieni ir labs beta glikānu avots.
Lietojot beta glikānus iekšķīgi, nav ziņots par blakusparādībām.
Lietojot uz ādas: beta glikāni ir droši, ja tos lieto īslaicīgi. Dažiem cilvēkiem tie var izraisīt ādas kairinājumu un/vai izsitumus.
Ja Jūs lietojiet medikamentus, tad atsevišķos gadījumos var būt mērena mijiedarbība starp zālēm un beta glikāniem.
- Zāles, kas samazina imūnsistēmas darbību (imūnsupresanti), mijiedarbojas ar beta glikāniem.
Beta glikāni var palielināt imūnsistēmas aktivitāti. Dažas zāles, piemēram, tās, ko lieto pēc orgānu transplantācijas, samazina imūnsistēmas aktivitāti. Beta glikānu lietošana kopā ar šīm zālēm var samazināt šo zāļu iedarbību.
- Zāles augsta asinsspiediena ārstēšanai (antihipertensīvie līdzekļi) mijiedarbojas ar beta glikāniem.
No auzām iegūtie beta glikāni var pazemināt asinsspiedienu. To lietošana kopā ar zālēm, kas pazemina asinsspiedienu, var izraisīt pārāk zemu asinsspiedienu. Lūdzu sekojiet līdzi sava asinsspiediena izmaiņām.
Bioloģiski aktīvi, droši un galvenokārt dabiski imūnsistēmas stimulatori ir meklēti visā cilvēces pastāvēšanas vēsturē. Daži no tiem, piemēram, beta glikāni, tiek intensīvi pētīti. Šobrīd jau ir vairāk nekā 15 000 publikācijas, tomēr meklējumi turpinās.
Beta glikāns - dabiskā augu izcelsmes molekula “modulē” (izmaina) imūnsistēmu, aktivizējot katru imūnsistēmas šūnu organismā: makrofāgus, neitrofilus, bazofilus, NK (natural killer) šūnas utt. Konkrēti, makrofāgi iedarbina virkni imūno funkciju, kas ļauj organismam radīt vispilnīgāko, efektīvāko un atbilstošāko iespējamo imūnreakciju. Ķermeņa imūno šūnu aktivitāte nosaka, cik labi imūnsistēma notver un uzveic “iebrucējus”, kas ir organismam nepiederoši. Beta glikāns iedarbina imūnās šūnas, lai tās būtu gatavas “cīnīties”.
Vienkārši sakot, beta glikāns ir katalizators, kas padara imūnsistēmu gudrāku, palielinot mūsu organisma aizsardzību. Pirmo reizi saskaroties ar patogēnu, imūnsistēma sākotnēji reaģē ātri un nespecifiski, izmantojot savu iedzimto imūno funkciju. Simptomi, kas saistīti ar šo reakciju, piemēram, sāpes un pietūkums, ir ķermeņa iekaisuma reakcijas rezultāts.
Tam seko lēnāka, specifiska reakcija uz patogēnu, ko veic imūnsistēmas adaptīvā puse. Adaptīvā imūnsistēma ir tā imūnsistēmas daļa, kurai ir ilgtermiņa atmiņa un kas neļauj daudziem patogēniem inficēt mūs vairāk nekā vienu reizi.
Imūnmodulējošās molekulas, no kurām dažas var uzņemt ar uzturu, var palīdzēt organismam aizsargāties pret patogēniem, pielāgojot normālu imūnreakciju, lai tā efektīvāk reaģētu, kad patogēns ir atklāts.
Konkrēti no rauga iegūtie beta glikānu veidi ietekmē neitrofilu un makrofāgu, šūnu, kas ir daļa no iedzimtas imūnsistēmas, iekaisuma un pretmikrobu aktivitātes. Ir jauni pierādījumi, ka rauga beta glikāni var "trenēt" ķermeņa imūnās šūnas efektīvāk reaģēt, kad tiek atklāts patogēns.
Šāda ķermeņa imūnsistēmas trenēšana ir atklāta samērā nesen – princips, kad iedzimtas imūnās šūnas saskaras ar specifiskiem mikrobiem (dzīviem vai nedzīviem), liekot šūnām efektīvāk reaģēt uz nākotnes draudiem. Būtībā tas nozīmē, ka iedzimtās imūnās šūnas pēc šiem “treniņiem” saglabā pieredzes “atmiņu”, kas ļauj tām ātrāk un efektīvāk reaģēt, kad tās sastopas ar citu patogēnu.
Galvenā atšķirība starp iedzimto imūno apmācību un tradicionālo imūno atmiņu ir “apmācītās” reakcijas plašais klāsts. Tradicionālajā imūnajā atmiņā imūnsistēma saskaras ar patogēnu (piemēram, masalām) slimības vai vakcinācijas laikā un adaptīvā imūnsistēma rada vairāku veidu specifiskas molekulas, lai atpazītu šo patogēnu (masalas) nākotnē un pasargātu organismu no inficēšanās.
Turpretim trenētā imunitātē iedzimtās imūnsistēmas sastapšanās ar dzīviem vai nedzīviem mikrobiem (“trenera” stimuliem) pielāgo iedzimto imūnreakciju, lai nodrošinātu efektīvāku reakciju pret patogēniem, kas nav saistīti ar “treneri”. Šis vispārinātais efekts ir būtisks imūnās aizsardzības nodrošināšanai, jo ir lietderīgi nodrošināt zināmu aizsardzības līmeni pret patogēniem, ar kuriem organisms nekad iepriekš nav saskāries.
Trenēta imunitāte, ko izraisa sākotnējā saskarsme ar treniņu stimulu, piemēram, rauga beta glikānu, izraisa pastiprinātu reakciju uz turpmākajām infekcijām. Vairākas dažādas imūnšūnu funkcijas ir sagatavotas ātrākai šī procesa aktivizēšanai, tostarp pretmikrobu molekulu ražošanai.
Ir iegūti pierādījumi tam, ka rauga beta glikāns varētu būt imūnsistēmas apmācības stimuls. Turklāt daži novērojumi no iepriekš publicētiem pētījumiem, kuros pētīts Wellmune® darbības mehānisms, atbilst iedzimta imūntrenera darbībai.
Apkopojot ieguvumus, secināms, ka beta-glikāni var pozitīvi mijiedarboties ar imūnsistēmu. Iespējamie beta-glikāna ieguvumi imūnsistēmai ir:
1) imūnās atbildes reakcijas palielināšana pret saaukstēšanos un gripu (uzlabo aizsardzību pret saaukstēšanos, gripu un citām elpceļu infekcijām);
2) sezonālo alerģijas simptomu mazināšana atsevišķos gadījumos (samazināta šķaudīšana un deguna aizlikums);
3) iekaisuma samazināšana intensīvas fiziskās slodzes dēļ: vairākos pētījumos beta-glikāni samazināja ar fizisko slodzi saistītu iekaisumu.
- Beta glikāni ir polisaharīdu cukurs, kas iegūts no rauga, sēnēm vai auzām. Tiem piemīt antioksidanta īpašības un tie ir ādu nomierinoši līdzekļi.
- Beta glikānu izpēte sākās pagājušā gadsimta 60. un 70. gados vienlaikus dažādos kontinentos. Galvenokārt ASV un Eiropā, tāpat Āzijā, lielākoties Japānā. Beta glikānu pētījumi Eiropā un Amerikā tika balstīti uz zināšanām par zimozāna, polisaharīdu maisījuma, kas izolēts no Saccharomyces cerevisiae šūnu sieniņām, imūnmodulējošo iedarbību.
- Āzijas medicīnā dažādu ārstniecisko sēņu (piemēram, šitaki, maitake, reiši u.c.) patēriņam ir senas tradīcijas. Detalizētos pētījumos par šo sēņu bioloģisko iedarbību, īpaši pretvēža iedarbību, tika konstatēts, ka beta glikāni ir galvenais nespecifiskās imūnmodulācijas cēlonis.
- Goro Čiharu no Teikjo universitātes Kavasaki, no šitaki sēnēm (Lentinula edodes) izolēja beta glikānu, kuru viņš nosauca par lentinānu.
- Visi pietiekami attīrīti polisaharīdi - imūnmodulatori izceļas ar ļoti zemu toksicitāti.
- Atšķirībā no vairuma citu dabisko produktu, attīrīti beta glikāni saglabā savu bioaktivitāti, kas ļauj apgalvot, ka beta glikāni darbojas šūnu un molekulārā līmenī.

C vitamīns
C vitamīns jeb askorbīnskābe ir būtisks mikroelements, kas nepieciešams normālai vielmaiņas darbībai, būtisks audu augšanai un atjaunošanai visā ķermenī. Tas ir ūdenī šķīstošs vitamīns, tomēr organisms pats to neražo. Kā antioksidants C vitamīns cīnās ar brīvajiem radikāļiem organismā, kas var palīdzēt novērst dažādas slimības un veicināt veselīgu novecošanos. C vitamīns darbojas kā “palīdzības molekula” vairākiem fermentiem, kas iesaistīti biosintēzē.
C vitamīna empīriskā formula ir C6 P8 O6. Tas ir kristālisks pulveris, baltā vai viegli dzeltenā krāsā, praktiski bez smaržas un ar ļoti skābu garšu. Kušanas temperatūra ir 190 grādi pēc Celsija. Vitamīna aktīvās sastāvdaļas parasti tiek iznīcinātas, termiski apstrādājot pārtiku, īpaši metālu, piemēram, vara, klātbūtnē. C vitamīnu var uzskatīt par nestabilāko no visiem ūdenī šķīstošajiem vitamīniem, taču tas tomēr var izturēt sasalšanu. Viegli šķīst ūdenī un metanolā, labi oksidējas, īpaši smago metālu jonu (vara, dzelzs u.c.) klātbūtnē. Saskaroties ar gaisu un gaismu, tas pakāpeniski kļūst tumšāks. Ja nav skābekļa, tas var izturēt temperatūru līdz 100°C. C vitamīns ir būtisks elements, kas jāuzņem ar uzturu, jo organisms to nespēj sintezēt . Tādējādi mūsu organisms ir izveidojis efektīvu adaptācijas sistēmu, kas uztur C vitamīna organiskās rezerves un novērš tā deficītu nepietiekama uztura gadījumā. Uztura saturošais C vitamīns askorbīnskābes reducētā veidā uzsūcas caur zarnu audiem, caur tievo zarnu, aktīvā transporta un pasīvās difūzijas ceļā, izmantojot SVCT 1 un 2 nesējus.
C vitamīns pirms uzsūkšanās nav jāsagremo. Ideālā gadījumā apmēram 80-90% no patērētā C vitamīna uzsūcas no zarnām. Tomēr C vitamīna uzsūkšanās spēja ir apgriezti saistīta ar uzņemšanu; tai ir tendence sasniegt 80-90% efektivitāti pie diezgan maza vitamīna daudzuma, bet šie procenti ievērojami samazinās, ja dienas deva pārsniedz 1 gramu. Ņemot vērā parasto devu, ko uzņemam ar ēdienu, 30–180 mg dienā, uzsūkšanās parasti ir 70–90% diapazonā, bet palielinās līdz 98%, ja deva ir ļoti maza (mazāk nekā 20 mg). Un otrādi, uzņemot vairāk nekā 1 g, uzsūkšanās mēdz būt mazāka par 50%. Viss process ir ļoti ātrs; organisms uzņem nepieciešamo apmēram divu stundu laikā, un trīs līdz četru stundu laikā neizmantotā daļa tiek izvadīta no asinsrites. Vēl ātrāk viss notiek cilvēkiem, kuri lieto alkoholu vai cigaretes, kā arī stresa apstākļos. Arī daudzas citas vielas un apstākļi var palielināt organisma vajadzību pēc C vitamīna: drudzis, vīrusu slimības, antibiotikas, kortizons, aspirīns un citi pretsāpju līdzekļi, toksīnu (piemēram, naftas produktu, oglekļa monoksīda) un smago metālu (piemēram, kadmijs, svins, dzīvsudrabs) iedarbība.
Faktiski C vitamīna balto asinsķermenīšu koncentrācija var sasniegt pat 80% no C vitamīna koncentrācijas plazmā. Tomēr organismam ir ierobežota C vitamīna uzglabāšanas jauda. Visizplatītākās uzglabāšanas vietas ir virsnieru dziedzeri (apmēram 30 mg), hipofīze, smadzenes, acis, olnīcas un sēklinieki. C vitamīns ir atrodams arī aknās, liesā, sirdī, nierēs, plaušās, aizkuņģa dziedzerī un muskuļos, kaut arī mazākos daudzumos. C vitamīna koncentrācija plazmā palielinās, palielinoties uzņemšanai, bet līdz noteiktai robežai. Jebkura 500 mg vai lielāka deva parasti tiek izvadīta no organisma. Neizlietotais C vitamīns tiek izvadīts no organisma vai vispirms tiek pārveidots par dehidroaskorbīnskābi. Šī oksidēšanās notiek galvenokārt aknās un arī nierēs.
Farmakokinētiskie eksperimenti ir parādījuši, ka C vitamīna koncentrāciju plazmā kontrolē trīs primārie mehānismi: uzsūkšanās zarnās, transportēšana audos un reabsorbcija nierēs. 100% uzsūkšanās efektivitāte tiek novērota iekšķīgi lietojot C vitamīnu devās līdz 200 mg vienā reizē. Kad askorbīnskābes līmenis plazmā sasniedz piesātinājumu, papildu C vitamīns galvenokārt tiek izvadīts ar urīnu.
Pirmie simptomi C vitamīna trūkumam organismā ir vājums un nogurums, muskuļu un locītavu sāpes, ātri zilumi, izsitumi mazu sarkanzilu plankumu veidā. Turklāt simptomi ir sausa āda, pietūkušas smaganas un mainījusies smaganu krāsa, smaganu asiņošana, brūču dzīšana, biežas saaukstēšanās, zobu izkrišana un svara zudums.
2013. gadā Eiropas Uztura zinātniskā komiteja paziņoja, ka vidējā C vitamīna nepieciešamība veselīgam līmenim ir 90 mg/dienā vīriešiem un 80 mg/dienā sievietēm. Ideāls daudzums lielākajai daļai cilvēku ir aptuveni 110 mg dienā vīriešiem un 95 mg dienā sievietēm. Pēc ekspertu grupas domām, šie līmeņi bija pietiekami, lai līdzsvarotu C vitamīna metabolisma zudumus un uzturētu plazmas askorbāta koncentrāciju aptuveni 50 µmol/L.
Smēķētājiem ieteicamā deva ir par 35 mg dienā lielāka nekā nesmēķētājiem, jo viņi ir pakļauti paaugstinātam oksidatīvajam stresam, ko izraisa cigarešu dūmu toksīni, un parasti tiem ir zemāks C vitamīna līmenis asinīs.
Šobrīd tiek ieteikts izvairīties no C vitamīna devām, kas pārsniedz 2 g dienā, lai novērstu blakusparādības (vēdera uzpūšanos un osmotisku caureju). Lai gan tiek uzskatīts, ka pārmērīgs askorbīnskābes patēriņš var izraisīt vairākas problēmas (piemēram, iedzimtus defektus, vēzi, aterosklerozi, paaugstinātu oksidatīvo stresu, nierakmeņus), neviena no šīm negatīvajām sekām uz veselību nav apstiprināta un tam nav ticamu pierādījumu. Tomēr ir zinātniski pierādījumi, ka liels C vitamīna daudzums (pieaugušajiem līdz 10 g/dienā) ir toksisks vai kaitīgs veselībai. Kuņģa-zarnu trakta blakusparādības parasti nav nopietnas un parasti izzūd, kad tiek samazinātas lielās C vitamīna devas. Biežākie C vitamīna pārdozēšanas simptomi ir caureja, slikta dūša, sāpes vēderā un citas kuņģa-zarnu trakta problēmas.
Daži medikamenti var pazemināt C vitamīna līmeni organismā: perorālie kontracepcijas līdzekļi, lielas aspirīna devas. Vienlaicīga C, E vitamīna, beta-karotīna un selēna uzņemšana var izraisīt holesterīna līmeni pazeminošo zāļu un niacīna efektivitātes samazināšanos. C vitamīns mijiedarbojas arī ar alumīniju, kas ir daļa no vairuma antacīdo līdzekļu, tāpēc starp to lietošanu ir nepieciešams pārtraukums. Turklāt ir daži pierādījumi, ka askorbīnskābe var samazināt dažu vēža un AIDS zāļu efektivitāti.
C vitamīnam (askorbīnskābei) ir svarīga loma normālā imūnsistēmas darbībā un tā izmantošana infekciju profilaksē un/vai ārstēšanā jau gandrīz gadsimtu ir ļoti piesaistījusi ārstu un pētnieku interesi. Ir labi zināms, ka C vitamīna deficīts izraisa lielāku uzņēmību pret infekcijām.
1970-tos gados Linus Pauling ierosināja, ka C vitamīns var veiksmīgi ārstēt un/vai novērst saaukstēšanos. Turpmāko kontrolēto pētījumu rezultāti ir bijuši nekonsekventi, izraisot neskaidrības un pretrunas, lai gan sabiedrības interese par šo tēmu joprojām ir augsta.
Vienā pētījumā tika pārbaudīti ar placebo kontrolēti izmeklējumi, kuros tika lietots 200 mg C vitamīna dienā, ko lietoja nepārtraukti kā profilaktisku ārstēšanu vai pēc saaukstēšanās simptomu parādīšanās. Profilaktiska C vitamīna lietošana kopumā nemazināja saaukstēšanās risku. Tomēr izmēģinājumos, kuros piedalījās maratona skrējēji, slēpotāji un karavīri, kas pakļauti ekstremāliem fiziskiem vingrinājumiem un/vai aukstā vidē, profilaktiska C vitamīna lietošana devās no 250 mg/dienā līdz 1 g/dienā samazināja saaukstēšanās biežumu par 50%. Visā populācijā profilaktiskā C vitamīna lietošana nedaudz samazināja saaukstēšanās ilgumu par 8% pieaugušajiem un 14% bērniem. Lietojot pēc saaukstēšanās simptomu parādīšanās, C vitamīns neietekmēja saaukstēšanās ilgumu vai simptomu smagumu.
Taču kopumā ir pierādīts, ka C vitamīns regulē imūnsistēmu pateicoties tā antioksidanta īpašībām un tā lomai kolagēna sintēzē, kas nepieciešama epitēlija barjeru stabilizācijai. Tāpat C vitamīnam ir loma fagocītiskajā funkcijā un tam ir imūnstimulējoša iedarbība uz limfocītiem. C vitamīna koncentrācija leikocītos ir ļoti augsta un tas tiek ātri izmantots infekcijas saslimšanas laikā. Faktiski tas tiek definēts kā leikocītu funkciju stimulators, īpaši neitrofilu un monocītu skaita kustības nodrošināšanai. Augsts C vitamīna līmenis neitrofīlos ir nepieciešams, lai neitralizētu ārkārtīgi augsto oksidatīvā stresa līmeni, kas ietver šūnu DNS un šūnu ķermeņu bojājumus, ko izraisa molekulas, kas pazīstamas kā reaktīvās skābekļa sugas (ROS), sauktas arī par “brīvajiem radikāļiem”. Antioksidantu līdzsvars ir svarīgs imūnās funkcijas noteicējs un imūnās šūnas ir īpaši jutīgas pret izmaiņām šajā līdzsvarā.
Tāpat C vitamīnam ir laba sinerģija ar imunitāti stiprinošām vielām, piemēram beta glikāniem. Beta glikānu spēcīgā imūnstimulējošā iedarbība ir labi pierādīta, jaunākie pētījumi liecina, ka dažām papildu bioaktīvām molekulām ir sinerģiska iedarbība, ja tās tiek kombinētas ar glikānu. Pirmkārt, vairāki zinātniski pētījumi ir apstiprinājuši labvēlīgo ietekmi, lietojot glikānu kombinācijā ar C vitamīnu. Galvenais iemesls, kāpēc C vitamīnam ir sinerģiska iedarbība, varētu būt fakts, ka C vitamīns stimulē tāda paša veida imūnās atbildes reakcijas kā glikāns.
Attiecīgi, varam secināt, ka C vitamīns ir būtiska viela, kas kalpo kā antioksidants un spēlē nozīmīgu lomu kā dažādu imūnsistēmas ceļu kofaktors (palīdz katalizēt bioķīmiskās reakcijas) un modulators.
- 20.gadsimta 40-tajos gados ārsts Frederiks Kleners izārstēja vējbakas, stingumkrampjus, cūciņu, masalas un poliomielītu, izmantojot C vitamīna terapiju.
- C vitamīns ir lieliski piemērots kolagēna atjaunošanai. Tas palīdz ādai izskatīties labāk un mazina kaulu sāpes.
- Skorbuts (cinga) bija slimība, ar kuru saskārās lielākā daļa jūrnieku. Ilgu laiku neviens nezināja, kā šo slimību ārstēt. Ap 1747. gadu, tika panākts izrāviens. Ārstam izdevās ar citrusaugļiem izārstēt 12 slimus jūrniekus. Tā bija vienīgā efektīvā ārstēšana un galu galā piešķīra jūrniekiem segvārdu “skābais”. Tas radās, sūcot laimus savā ceļojumā, lai novērstu slimību.
- C vitamīns ir nepieciešams pareizai tauku vielmaiņai. Būtībā tas ļauj ķermenim izmantot taukus kā degvielu. Ir arī pierādīts, ka C vitamīns var palīdzēt samazināt apetīti.
- Izmantojot C vitamīnu, šķīstošo kafiju un sodu var attīstīt melnbaltās kinofilmas.
- Cilvēki, primāti un jūrascūciņas ir vienīgie zīdītāji, kas paši nespēj ražot sev organismā C vitamīnu.

L-glutamīns
Glutamīns ir svarīga aminoskābe, kas ietekmē visu, sākot no imunitātes līdz ķermeņa atjaunošanās spējām pēc traumām. Glutamīns palīdz veidot organismam citas aminoskābes, kā arī palīdz ražot glikozi. Glutamīnam ir būtiska nozīme bojāto audu atjaunošanā, kolagēna ražošanas stimulēšanā un jaunu šūnu augšanas veicināšanā. Faktiski veselās šūnas, kas strauji vairojas, izmanto glutamīnu kā enerģijas ieguves avotu.
Glutamīns ir visbiežāk sastopamā un daudzpusīgākā brīvas formas (jau sašķelta un viegli uzsūcas) α-aminoskābe mūsu organismā. Organismā glutamīns veidojas no glutamīnskābes, fermenta glutamīnsintetāzes iedarbībā, piesaistot amonjaku. Glutamīns ir svarīga slāpekļa vielmaiņas sastāvdaļa. Tāpat kā arginīns, glutamīns ir bioķīmiskais slāpekļa donors, veidojoties citām aminoskābēm, purīniem un pirimidīniem. Piemēram, in vitro un in vivo pētījumos ir konstatēts, ka glutamīns ir būtiska viela, lai attīstītos audi un veidotos jaunas galvenās imūnšūnas – limfocīti. Glutamīns palīdz ražot citokīnus – bioķīmiski aktīvas imūnās sistēmas savstarpējās saziņas proteīnu molekulas, ko imūnās sistēmas šūnas ražo, lai iedarbotos uz citām imūnšūnām. Šie citokīni aktivē vai modulē iedzimtās imūnās sistēmas šūnas (makrofāgus, dendrītiskās šūnas, dabiskās galētājšūnas) un arī epitēlijšūnas. Imūnās šūnas glutamīnu patērē gan, ja organisms ir vesels, gan slimības gadījumā, un šis patēriņš ir līdzīgs vai lielāks nekā glikozes patēriņš.
Glutamīns ir iesaistīts dažādos bioķīmiskos procesos. Daži no tiem nodrošina enerģiju, kas kalpo kā aminoskābju sintēzes prekursors, slāpekļa donors nukleīnskābju veidošanās procesā, kas palīdz sintezēt intracelulāras olbaltumvielas un darbojas kā būtisks atbalsts skābju-bāzes līdzsvarā.
Glutamīns ir arī potenciāls prekursors N-acetil-glikozamīna un N-acetil-galaktozamīna sintēzē, kam var būt izšķiroša nozīme zarnu mucīna (glikoproteīns) sintēzē un, līdz ar to, pasīvās barjeras uzturēšanā pret baktēriju invāziju.
Vienkārši runājot, tā ir "barība" enterocītiem (šūnām, kas veido tievo zarnu), palīdzot dziedēt zarnu iekaisumu. Tas ir lieliski piemērots autoimūnām slimībām, kas bieži pastiprinās zarnu iekaisuma gadījumā. Ir gadījumi, kad glutamīna papildus lietošana mazina psoriāzi, ekzēmu un locītavu sāpes. Ja zarnu mikrobioma testā ir konstatēti iekaisuma marķieri, glutamīns var būt noderīgs.
Medikamenti, kurus lieto, lai novērstu krampjus (pretkrampju līdzekļi), mijiedarbojas ar glutamīnu.
Dažiem cilvēkiem glutamīns var palielināt krampju risku. Tāpēc glutamīna lietošana var samazināt krampju profilaksei lietoto zāļu iedarbību.
Lietojot iekšķīgi, glutamīns ir drošs, ja to lieto devās līdz 40 gramiem dienā. Blakusparādības parasti ir vieglas un var ietvert vēdera uzpūšanos, sliktu dūšu, reiboni, grēmas un sāpes vēderā.
Aknu slimību gadījumā glutamīns var palielināt smadzeņu darbības traucējumu risku cilvēkiem ar progresējošām aknu slimībām. Konsultējieties ar savu veselības aprūpes speciālistu, ja Jums ir kāda progresējoša aknu slimība.
Bipolāri traucējumi: glutamīns var palielināt mānijas vai hipomānijas risku cilvēkiem ar šo stāvokli.
Mononātrija glutamāta (MSG) jutība: ja esat jutīgs pret MSG, iespējams, esat jutīgs arī pret glutamīnu, jo ķermenis pārvērš glutamīnu par glutamātu.
Uzturvielas var ietekmēt un regulēt šūnu vielmaiņu un šūnu darbību, kas ir īpaši svarīgi dažādu imūnsistēmas apakšgrupu aktivizēšanai un darbībai. No svarīgākajām barības vielām imūno šūnu funkcijai ir glutamīns, iespējams, visizplatītākais atzītais imūnelements, spēlējot galveno lomu TCA ciklā (trikarbonskābes cikls - šūnu elpošana, kas ietver virkni ķīmisku reakciju, kas atbrīvo uzkrāto enerģiju), proteīnu reakcijās un antioksidantu procesos.
Ja runājam par imunitāti, tad nevaram nerunāt par zarnu traktu. Kāpēc? Daudzus gadus zarnas tika pētītas tikai kā gremošanas, barības vielu absorbcijas un fermentācijas orgāns. Tomēr tagad ir zināms, ka zarnu trakts ir sarežģīts orgāns, kas veic dažādas kritiskas fizioloģiskās funkcijas. Zarnu gļotāda satur ne tikai sekrēcijas, bet arī imūnās un neiroendokrīnas šūnas absorbējošus enterocītus (epitēlija šūna zarnu gļotādā, kurai ir, galvenokārt, barības vielu absorbējoša nozīme). Viens epitēlija slānis, kas pārklāj kuņģa-zarnu traktu, rada selektīvu barjeru, lai novērstu kaitīgo vielu, piemēram, toksīnu, alergēnu un patogēnu iekļūšanu lielajā asinsrites lokā.
Šādā griezumā skatoties, varam saprast glutamīna nozīmīgo lomu. Glutamīns ir galvenā enterocītu enerģijas viela. Šūnām, strauji daloties, ir nepieciešams glutamīns, kas kalpo kā slāpekļa donors, aminoskābēm, purīnam un pirimidīnam, iedarbojoties uz karbamoilfosfāta sintetāzi.
Pamatojoties uz šo, glutamīns parasti ir iekļauts to “imūnelementu” sarakstā, kuriem ir bioloģiska iedarbība.
Secinājums: glutamīns ir nepieciešams imūnsistēmas šūnām gan kā primārā izejviela, gan kā oglekļa un slāpekļa donors nukleotīdu prekursoru sintēzei. In vivo pētījumi ir parādījuši, ka glutamīns ir būtisks monocītu, limfocītu un neitrofilu imūnšūnu optimālai darbībai. Vairākos pētījumos ar pacientiem ir novērota infekcijas saslimstības uzlabošanās, ja tie saņem glutamīnu.
- Kāposti un bietes satur augstu glutamīna koncentrāciju. Citi pārtikas avoti ir zivis, pupiņas un piena produkti.
- Atšķirībā no proteīna vai kreatīna, glutamīns tiešā veidā nepalīdz veidot muskuļu masu.
- Ja ir sanācis pavadīt vairāk laika sporta zālē, glutamīns palīdz atgūties no sāpēm muskuļos un noguruma, tādējādi samazinot “atgūšanās” laiku starp treniņiem.
- Pietiekams glutamīna daudzums organismā veicina labu zarnu “gļotādas integritāti”, kas nozīmē, ka tām veidojas spēcīga aizsardzība pret tādiem kairinātājiem kā, piemēram, alkohola, narkotikām vai aspirīna.
- L-glutamīnu vislabāk ir lietot apmēram 10-15 minūtes pirms ēšanas tukšā dūšā, un lietot 2-3 reizes dienā (tātad pirms 2-3 ēdienreizēm dienā), lai sniegtu atbalstu vienmērīgi un pastāvīgi.
- Vajadzētu izvairīties no glutamīna lietošanas kopā ar kaut ko karstu, piemēram, kafiju, tēju, zupu vai buljonu. Galvenais iemesls tam ir tas, ka karsta temperatūra var denaturēt (atņemt dabiskās īpašības) vai sabojāt aminoskābes.

Melnais plūškoks (Sambucus nigra L.)
Melnajam plūškokam (Sambucus nigra L.) ir sena vēsture daudzās atšķirīgās kultūrās, lai ārstētu vīrusu infekcijas, un pašlaik tas ir viens no visvairāk izmantotajiem ārstniecības augiem visā pasaulē. Plūškoka ekstraktam ir pierādītas pretvīrusu un pretmikrobu īpašības un tā lietošanas drošība ir vispāratzīta.
Melnais plūškoks (Sambucus nigra L.) ir viena no daudzām plūškoku sugām. Melnais plūškoks ir līdz 6 m augsts koks vai krūms. Tam ir krēmbalti ziedi vairogveidīgās ziedkopās un melnvioleti kauleņi ar trim kauliņiem. Ziedi zied jūnijā un jūlijā. Lapas pretējas, nepāra plūksnaini saliktas no 3, 5 vai 7 lapiņām. Dabiskais izplatības areāls ir Dienvideiropa, Ziemeļāfrika un Tuvie Austrumi.
Plūškoka ogas satur daudzas aktīvas ķīmiskas vielas, kam piemīt farmakoloģiska aktivitāte, tostarp antocianīnus (galvenokārt cianidīna 3-glikozīds un cianidīna 3-sambubiosīds), kas, kā pierādīts, stiprina imūnsistēmu un uzrāda pretvīrusu iedarbību. Perorālas plūškoka lietošanas rezultātā šo antocianīnu līmenis ir konstatēts asins plazmā.
Citas sastāvdaļas ir vitamīni un minerālvielas nelielos daudzumos un ogļhidrāti, piemēram, pektīns un līdz 7,5% glikozes un fruktozes.
Bez jau minētām plūškoka bioaktīvām sastāvdaļām, tas satur arī dažādus (poli)fenola savienojumus un terpenoīdu savienojumus. Polifenoli, kas pazīstami ar savu spēju neitralizēt brīvo radikāļu aktivitāti, kopā ar antocianīniem ir vissvarīgākās bioloģiski aktīvo savienojumu grupas, kas atrodas plūškokā salīdzinoši augstā koncentrācijā.
Jaunākie pētījumi gan liecina, ka dažas pārtikas pārstrādes metodes var ietekmēt bioloģiski aktīvo savienojumu saturu plūškokā, kā arī ķīmiskais sastāvs ir atkarīgs no dažādiem faktoriem, piemēram, atrašanās vietas, nogatavošanās stadijas un klimatiskajiem apstākļiem. Piemēram, sulu, kas plaši tiek lietota gan uztura bagātinātājos, gan sīrupos, ražošanas metode ietekmē bioaktīvo savienojumu saturu. Plūškoka sulas, kas apstrādātas ar fermentatīvo apstrādi (pektinolīzi), uzrādīja zemāku lielāko daļu pētīto fenola savienojumu saturu, salīdzinot ar sulām, kas ražotas bez fermentatīvās apstrādes. Tādēļ izvēloties uztura bagātinātajus ar plūškoka sulu vai ekstraktu, ir jāpievērš uzmanība aktīvo vielu (polifenolu un antocianīnu) standartizācijai. Plūškokam piemīt dažādas ārstnieciskas īpašības in vitro un in vivo, tostarp antioksidanta, pretiekaisuma, pretvēža, pretgripas, pretmikrobu, pretdiabēta, sirds un asinsvadu aizsardzības un neiroprotektīvas aktivitātes. Tomēr plūškoku galvenokārt lieto, lai ārstētu parastos simptomus, kas saistīti ar saaukstēšanos: drudzi, klepu, aizliktu degunu, iesnas un gripu, kā arī profilaktiski imūnsistēmas stiprināšanai.
Plūškoka miza, nenogatavojušās ogas un sēklas satur nelielu daudzumu vielu, kas pazīstamas kā lektīni, kas var izraisīt kuņģa darbības traucējumus, ja tās tiek ēstas pārāk daudz . Turklāt plūškoks satur vielas, ko sauc par cianogēniem glikozīdiem, kas dažos gadījumos var izdalīt cianīdu. Tas ir toksīns, kas atrodams arī aprikožu sēklās un mandelēs. Tomēr tā saturs nav augsts - 3% no aplēstās letālās devas 60 kg smagai personai jeb precīzāk tā daudzums ir 3 mg uz 100 gramiem svaigu ogu un 3–17 mg uz 100 gramiem svaigu lapu.
Taču svarīgi ir zināt, ka komerciālie preparāti un vārītas ogas nesatur cianīdu. Nevārītu ogu, lapu, mizas vai plūškoka sakņu ēšanas simptomi ir slikta dūša, vemšana un caureja.
Plūškokam nav zināma smaga, nopietna vai mērena mijiedarbība ar medikamentiem. Nelietojiet plūškoku saturošus preparātus, ja ir novērota alerģiska reakcija.
Ir pierādīts, ka melnā plūškoka ekstrakti un ziedu uzlējumi palīdz samazināt gripas smagumu un ilgumu. Pētījumā, kurā piedalījās 312 avioceļotāji, kuri trīs reizes dienā lietoja kapsulas, kas satur 300 mg plūškoka ekstrakta, atklājās, ka saslimušajiem bija īsāks slimības ilgums un simptomi nebija tik smagi.
Pētījumos ir konstatēts, ka plūškoks ir efektīvs pret dažādiem patogēniem, piemēram Helicobacter pylori baktēriju (var izraisīt kuņģa čūlu, sāpes vēderā, nelabumu), Streptococcus pyogenes (biežākais faringīta bakteriālais cēlonis) C un G grupas Streptococci, Branhamella catarrhalis (var izraisīt cilvēku elpošanas sistēmas, vidusauss, acu, centrālās nervu sistēmas un locītavu infekcijas) un Haemophilus influenza (var izraisīt pneimoniju, otītu, sinusītus, laringotraheītu, bronhītu).
Pētot standartizēta plūškoka ekstrakta imūnmodulējošo iedarbību pret leišmaniozes un malārijas infekcijām, tika konstatēta aizkavēta slimības attīstība.
Melnajam plūškokam ir daudz biokatīvu sastāvdaļu, kas ir labvēlīgas vispārējam veselības stāvoklim un ir saistītas ar plaša spektra veselības traucējumu atvieglošanu, attiecīgi plūškoks ir daudzsološs zema riska gripas un citu vīrusu ārstēšanai un ne-vīrusu patogēniem – un, iespējams, arī kā akūtu vīrusu infekciju profilakses līdzeklis.
- Kādreiz plūškoku uzskatīja par svētu koku, jo tas aizsargājot no daudzām briesmām un nelaimēm – ugunsgrēkiem, ļauniem cilvēkiem, pat no laupītājiem un, protams, daudzām slimībām un kaitēm.
- Plūškoki jau ir “pieauguši” pēc 3–4 gadiem. Plūškoka augļi nav piemēroti mehāniskai ražas novākšanai, jo tie grūti atdalās no kātiņiem, tomēr dažās valstīs tos ievāc, izmantojot tehniku, kas paredzēta citām ogu kultūrām un pielāgota plūškokam.
- Plūškoka vēsture aizsākās jau 400. gadā pirms mūsu ēras, kad Hipokrāts, "medicīnas tēvs", nosauca šo koku par savu "ārstniecības lādi".
- Plūškoka ziedi, augļi un lapas ir lieliski antioksidantu avoti. Piemēram, vienam no ogās atrodamajiem antocianīniem ir 3,5 reizes lielāka antioksidanta spēja nekā E vitamīnam.
- Plūškoka ogas var samazināt urīnskābes līmeni asinīs. Paaugstināts urīnskābes līmenis ir saistīts ar paaugstinātu asinsspiedienu un negatīvu ietekmi uz sirds veselību
 Bezmaksas piegāde uz Omniva pakomātiem visā Baltijā pirkumam no 20 eur!
Bezmaksas piegāde uz Omniva pakomātiem visā Baltijā pirkumam no 20 eur!